放化疗要补什么样的硒(化疗补硒)

硒是人体必需的重要微量元素,被国内外医药界和营养学界称为“生命的火种”“长寿元素”“抗癌之王”“心脏守护神”“天然解毒剂”等。
功能化纳米硒作为一种新型单质、元素硒,与无机硒等其他硒形态相比具有更高的生物利用度、更好的生物活性和更高的安全性,且具有良好的抗氧化、抗肿瘤和免疫调节作用。
本文概述了纳米硒在生物医药中的应用,纳米硒的功能化和靶向修饰增强抗肿瘤效果,含硒纳米材料在抗肿瘤中的应用,介绍了纳米硒制剂产业化发展现状及其未来前景。
生物技术和纳米技术的结合引发了癌症纳米技术的发展,可以应用于靶向治疗、分子诊断和分子成像。
硒是人体必需的重要微量元素之一,具有良好的抗氧化、抗肿瘤和免疫调节作用。硒作为药物用于肿瘤治疗已经得到越来越多的研究,但硒化合物作为一种有机硒制剂,其毒性较高,靶向性较差。
纳米硒(Selenium Nanoparticles,SeNPs)作为一种新型单质、元素硒,具有更高的生物利用度、更强的生物活性和更低的毒性,作为“治疗性药物载体”,具有生物相容性好、负载率高、毒性低、易合成、易储存等优点。

纳米硒在多模态肿瘤诊断与治疗上的应用
纳米硒以及含硒纳米材料在生物医药中的应用
尽管化疗已被广泛应用于癌症的治疗,但如何最大限度提高其治疗效果,最大限度减少对正常组织的损害仍是一个挑战。
多功能复合纳米材料与传统的药物制剂相比具有诸多优势,可有效提高纳米粒子对肿瘤的诊疗效果。
化疗和光热联合治疗已成为一种很有前途的癌症治疗方法。然而,精确递送的复杂性和在特定肿瘤部位启动药物释放的能力仍是一个具有挑战性的难题。
陈填烽课题组设计并成功合成了双靶点多肽负载阿霉素和吲哚菁绿的功能化硒纳米颗粒SeNPs-DOX-ICG-RP。双靶向设计增加了细胞摄取,延长了循环时间,提高了化疗和光热联合治疗的效率。
Wang等研究制备的多刺激肿瘤靶向药物载体Se@SiO2-FA-CuS/DOX纳米复合材料,在体内外均能有效地抑制肿瘤细胞的生长,甚至完全消除肿瘤,且治疗没有明显的不良反应。
Deng等设计制备了牛血清白蛋白负载SeNPs/吲哚青绿纳米颗粒BSINPs,具有良好的分散性、合适的尺寸、荧光稳定性和特征光谱等特性,是非常理想的化疗-光热联合治疗癌症的纳米材料。

BSINPs的制备及化学-光热联合治疗示意
为了更进一步提高放疗的治疗效果,研究人员已经提出了许多策略,通过放疗增敏来增强放疗的效果。
目前,以X射线为基础的放射治疗是治疗癌症最有效的方法之一,而辐射抗性和严重的副作用是一个具有挑战性的问题。
陈填烽课题组以聚乙二醇(PEG)为表面修饰剂和模板制备出的PEG-SeNPs纳米系统,通过X射线表现出显著的放射增敏作用。此外,课题组发现硒二唑衍生物通过引起DNA损伤和活性氧(ROS)过量产生从而导致蛋白激酶B(AKT/PKB)和细胞外调节蛋白激酶(ERK)失活,通过G2/M期阻滞来增强辐射诱导对A375黑色素瘤细胞的生长抑制作用。
临床数据显示低剂量硒可能对正常组织有辐射保护作用,但不清楚当暴露于高浓度但无毒的亚硒酸盐时,硒对肿瘤细胞是否有增敏或保护作用。
陈填烽等发现SeNPs联合照射对MCF-7乳腺癌细胞的杀伤作用大于单纯照射,并使细胞自噬、细胞周期阻滞于G2/M期,ROS水平升高,说明纳米硒的辅助应用可提高乳腺癌放射治疗的疗效。
新一代纳米放射增敏剂的开发不仅可以增强肿瘤组织的放射增敏作用,而且可以提高健康组织的放射抵抗力。
Du等设计并合成聚乙烯基裂解烯醚酮和硒代半胱氨酸修饰的Bi2Se3纳米粒子的新型多功能热敏剂,可同时增强放疗治疗效果并降低其毒性。
放化疗作为一种放疗和化疗相结合的方法,已被提出用来减少对肿瘤周围组织的损伤,提高实体肿瘤的放射敏感性。
陈填烽课题组设计并合成FA@SeNPs作为肿瘤靶向剂,125I粒子与FA@SeNPs联用表现出显著的协同效应,这种联合治疗显示出更好的体内抗肿瘤活性和较低的全身毒性。

功能化纳米硒作为125I粒子放射治疗增敏剂的模型
此外,陈填烽课题组设计和制备了Au@Se-R/ANCs作为纳米增敏剂来实现高效的协同癌症放化疗,和X射线联合应用可以显著抑制肿瘤生长,且未观察到急性毒性。
Zhang等成功制备了聚乙二醇化硒纳米颗粒(PSNP),与X射线联合应用对肺癌细胞表现出有效的抗癌作用。
近年来,通过不同的靶向策略,利用肿瘤内部的微环境进行特殊性的响应有很好的发展,药物在生物体内的利用率得到大幅度的提高,一些药物的毒副作用被降低。
通过在纳米硒的表面修饰某些多糖蛋白,可以增强纳米硒的细胞吸收以及抗肿瘤效果。
陈填烽课题组利用螺旋藻多糖(SPS)、多糖-蛋白复合物(PSP)、壳聚糖(CS)等对纳米硒进行表面修饰,增强了癌细胞对纳米硒的细胞吸收。

多糖蛋白复合物修饰SeNPs的合成示意
肿瘤分子靶向药物可利用肿瘤细胞与正常细胞之间分子生物学上的差异,抑制肿瘤细胞的生长增殖,使其死亡。

转铁蛋白(Tf)是一种靶向配体,能够将大量治疗药物输送到恶性肿瘤部位,有效增强药物的利用浓度,且Tf/TfRs介导的内吞作用能有效增强肿瘤对药物的积累效果。
陈填烽课题组利用Tf修饰的纳米硒,负载DOX可作为一个有效的靶向策略,增强肿瘤细胞对纳米硒的吸收以及协同化疗的功效。
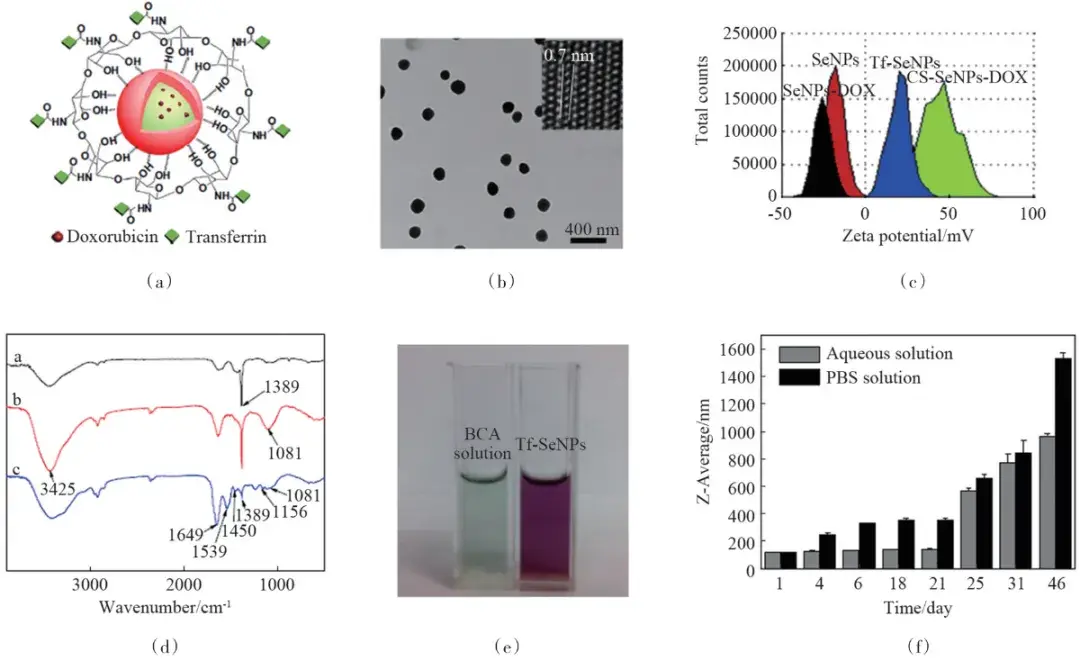
Tf-SeNPs-DOX的表征数据
叶酸受体(FAR)可通过受体介导的内吞作用将捕获的药物转运到细胞中,增加癌细胞中药物的浓度,且叶酸(FA)靶向药物可以针对特定的癌细胞。
陈填烽课题组设计合成FA修饰的纳米硒,通过FAR介导的内吞作用,显著增强细胞对SeNPs的摄取。课题组还设计并合成了多功能黄芩苷(B)和FA表面修饰的硒纳米粒子(B-SeNPs-FA),用于靶向治疗乙型肝炎病毒感染的肝癌。
此外,课题组通过半乳糖胺(GAL)表面修饰构建了功能化冰片(Bor)修饰的SeNPs负载抗癌药物Fe(PiP)3多功能纳米体系,表现出优异的血液相容性和抗癌活性,且有效延长了包封药物的循环时间。
人表皮生长因子受体2(HER2抗原)在多种人类恶性肿瘤中过表达,抗HER2抗原的人源化单克隆抗体曲妥珠单抗(HER2)可用作设计膀胱癌等靶向纳米药物的生物标志物。
陈填烽课题组构建由含有二硫键的HER2作为表面修饰剂组成的顺序触发的纳米体系可以精确递送药物并同时抑制癌症生长、迁移和侵袭。
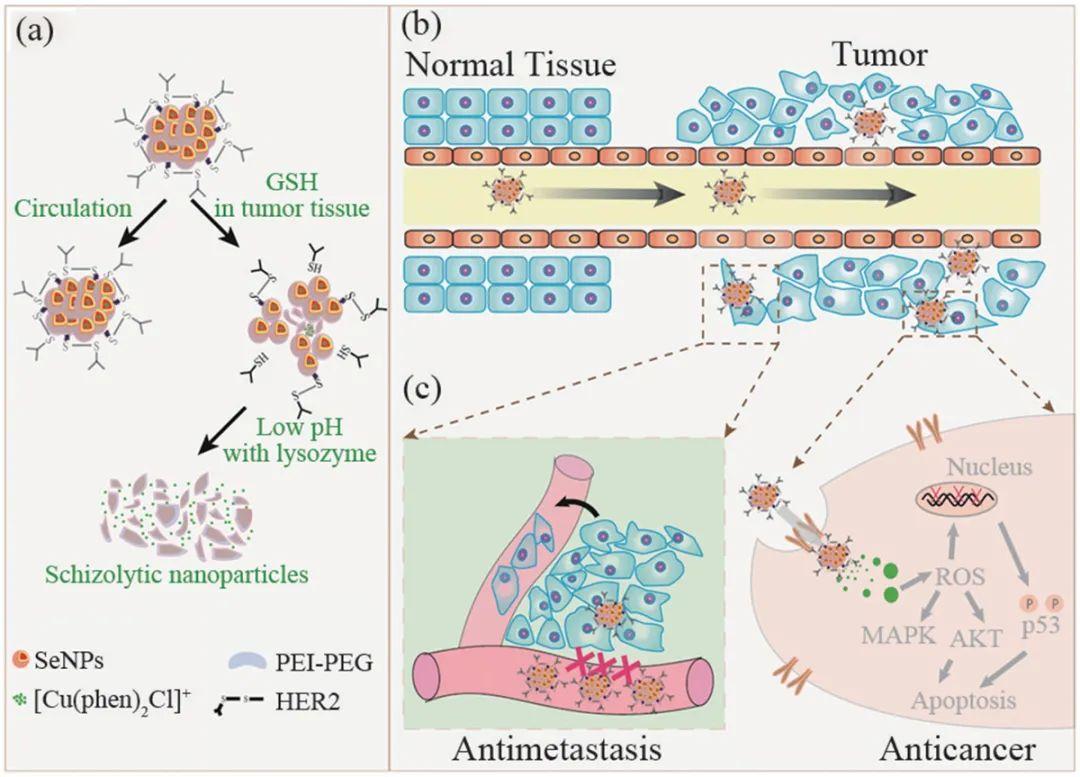
合理设计顺序触发的纳米系统,用于精确的药物释放和同时抑制肿瘤的生长、迁移和侵袭
整合素αvβ3在大多数恶性肿瘤中过表达,陈填烽课题组利用龙须菜多糖(GLP)对整合素较强的亲和力以及在H2O2条件下降解的特性修饰纳米硒,延长纳米硒在体内的循环时间,达到更好的细胞吸收效果以及癌症靶向性和抗肿瘤效果。
αvβ3和αvβ5整合素可被多肽序列Arg-Gly-Asp(RGD)特异性识别,其在肿瘤血管系统中过表达。
陈填烽课题组设计合成载有DOX的靶向SeNPs(RGD-SeNPs),RGD肽表面装饰增强了SeNPs的细胞摄取和抗血管生成活性。
此外,课题组合成了藻蓝蛋白(Phycocyanin,PC)功能化的硒纳米粒子(PC-SeNPs),通过调节纳米粒子的尺寸和PC含量实现了最有效的保护作用。
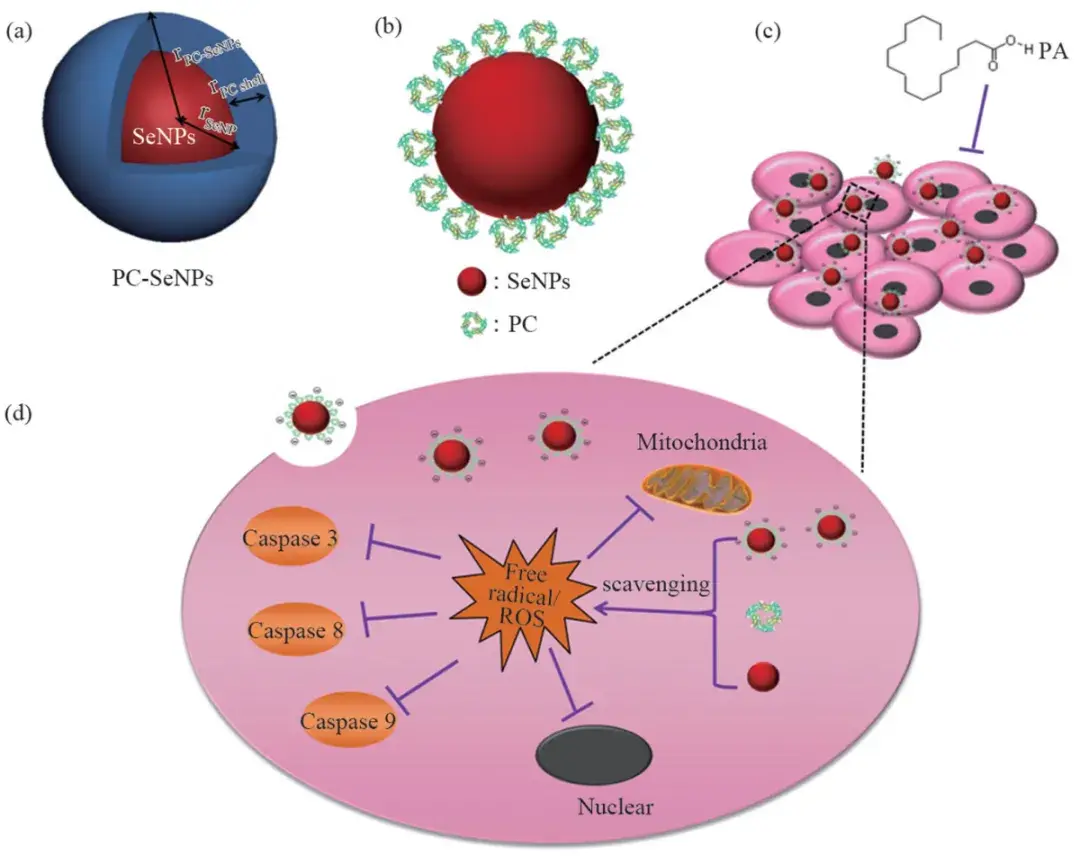
合理设计PC-SeNPs以保护INS-1E细胞免受氧化损伤及其机制
(a)PC-SeNPs的核壳结构;(b)PC-SeNP的模拟结构;(c)(d)PC-SeNPs的作用机制:对PA诱导的INS-1E细胞的保护作用PARP裂解
表皮生长因子受体(EGFR)在超过80%的鼻咽癌患者中高表达,并且预后不良。
西妥昔单抗(Cet)是一种阻断EGFR的人-鼠嵌合抗体,可抑制肿瘤细胞生长/存活、转移以及血管生成。
陈填烽课题组利用EGFR为靶向分子,设计合成了高度均匀、稳定以及具有EGFR靶向和肿瘤微环境响应能力的硒纳米粒子用于鼻咽癌的诊断和治疗。
另外,课题组通过结合超小硒纳米颗粒和贝伐珠单抗(Av)设计了一种智能有效的纳米体系,用于癌症的同时放射治疗和抗血管生成治疗。
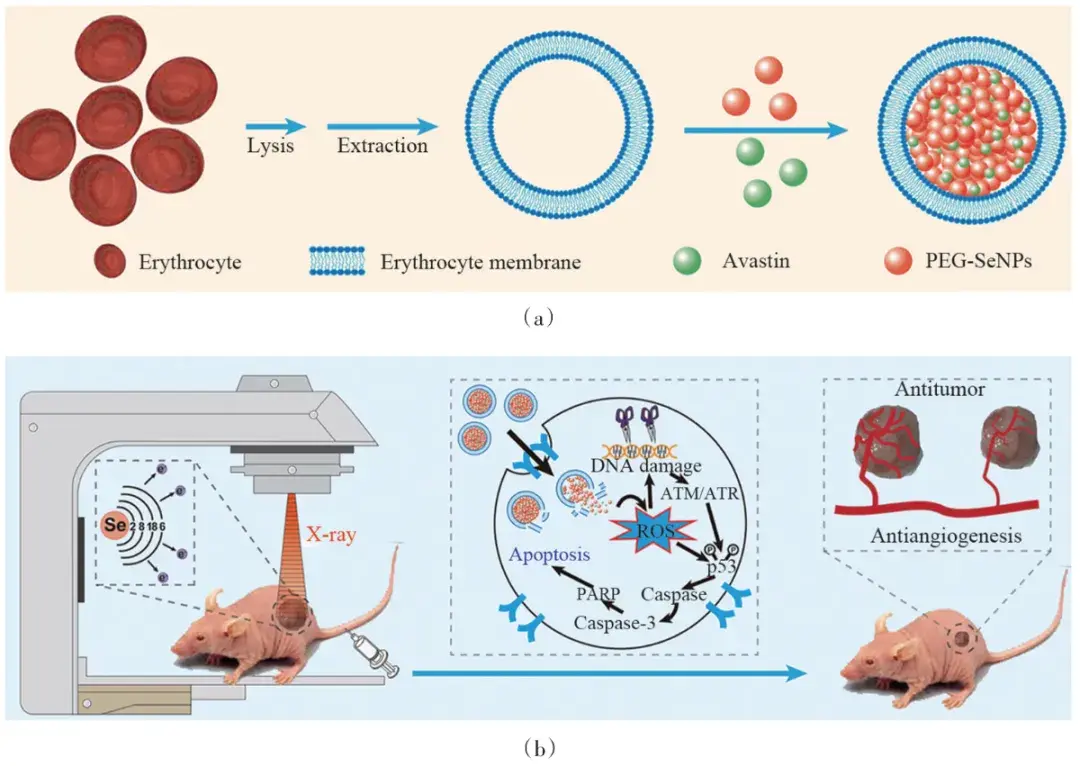
RBCs@Se/Av的合理设计可以同时提高癌症的放射治疗效率和抗血管生成
大剂量的化疗会对正常组织和免疫系统产生严重的毒性,靶向与多药物协同抗肿瘤能有效改善肿瘤治疗中药物剂量依赖问题,具有避免意外靶向和发挥协同抗癌药物活性的潜力。
Yu等利用介孔氧化硅作为SeNPs上的包覆层,可以提高药物阿霉素的包载量,同时设计构建了隐蔽性抗癌叶酸靶向的纳米载体,为高载药量提供了一个宽敞的储液库。
近年来,硒作为协同抗癌药物的研究日渐增多,硒和非甾体抗炎药(NSAID)舒林酸的组合可显著抑制肠道肿瘤的发生,使肿瘤发生率降低52%,肿瘤多发性降低80%。
硒联合用药的研究也越来越多,比如硒联合光热疗法、DOX化学疗法的三重治疗等。当纳米复合材料在肿瘤部位高度富集时,近红外激光照射产生热,可有效消融肿瘤;同时DOX和Se从纳米复合材料中释放出来进行协同化疗,可以长时间杀死肿瘤细胞并抑制其转移。
纳米硒粒子可以长时间抑制癌细胞生长,但无法在短时间内有效消除实体瘤,亟需通过硒纳米粒子结合其他方式快速直接消除肿瘤。
通过生物组织相容性纳米颗粒作为载体来释放抗肿瘤药物是一种高效的治疗手段,目前已经用于组织修复和癌症治疗等方面,但是如何诱导纳米颗粒释放药物来抑制肿瘤仍不清楚。
Wang等设计合成的具有生物可降解性、pH敏感性掺杂羟基磷灰石的硒纳米粒子(Se-HANs),可以潜在填补骨肿瘤去除后所产生的骨缺陷,来并通过半胱天冬氨酸依赖型凋亡途径诱导肿瘤细胞凋亡以抑制肿瘤形成。
Zdeněk课题组通过聚山梨酯20作为表面活性剂,合成了不同尺寸的SeNPs。在低Se浓度下,SeNPs对常见细菌具有明显的抗菌活性。
Ghada等利用地衣芽孢杆菌自由细胞上清液处理1 mM SeO2进行生物合成,研究中产生的SeNPs可用作预防食源性病原体形成生物膜的药物。
Shafkat等利用大蒜提取物中从亚硒酸钠溶液中合成SeNPs,在此过程中合成的硒纳米颗粒对病原菌具有有效的抗菌活性。
Andrea课题组研究SeNPs的大小对哺乳动物细胞毒性和抗菌功效的影响,抗菌活性显示出强烈的大小依赖性,SeNPs具有取决于其大小的多模式作用机制。
用于抑制肿瘤细胞生长的硒基复合物均可以通过复合物本身或对应代谢物展示出显著且独特的氧化还原活性。
通过设计合成Ru-BSE的含硒化合物,增强了硒二唑衍生物的溶解性,从而使细胞摄取更多药物。生物素修饰的靶向Ru-BSE可以在肿瘤部位特异性地积聚,从而增强抗肿瘤的效力,并最大限度减少不良毒性副作用。
负载硒代半胱氨酸和转化生长因子-β抑制剂的纳米材料,则可以增强基于自然杀伤细胞的肿瘤免疫疗法的效果。
富硒藻蓝蛋白是一种利用螺旋藻生物富集硒方法得到的产物,激光辐照含硒藻蓝蛋白(Se-PC)后产生ROS并触发不同途径的细胞死亡,在正常组织中,降解的PC肽和激光照射促进酶合成SOD,参与GSH-Px合成,都有助于防止肿瘤生长。
而且,纳米硒能发挥很好的抗肿瘤免疫治疗效果,显著增强基于细胞因子诱导的杀伤细胞的免疫治疗效果。
无机硒高毒性的缺点可以通过多糖修饰解决,香菇多糖是被中国批准的抗癌药物,可与硒酸结合转化为酯复合物。硒-香菇多糖复合物可以显著抑制黑素瘤和结肠癌的生长和转移,且较亚硒酸钠毒性更低。
纳米硒制剂的产学研转化
缺乏高效低毒、结构简单、成药性高的纳米材料;难以突破从实验室走向工业化生产的技术这2个瓶颈极大限制了纳米医药从基础走向临床,成为纳米医学领域的前沿热点及“卡脖子”问题。
寻找高效低毒、生物相容性好、成药性高的纳米材料是纳米医学领域亟待解决的关键科学问题。
如何根据硒的化学特性进行化学形态及剂型改造,在此基础上突破工业化生产和制造的瓶颈,是一个重要的科学技术难题。
通过产学研合作,暨南大学与广东暨创硒源纳米研究院有限公司合作,利用多种药品/食品来源的生物分子,通过大分子表面修饰纳米硒,并对合成工艺进行长期摸索与改进,突破工业化生产的关键技术,开发成一套独有的纳米硒一体化生产工艺。
并在此基础上,进一步优化纳米硒生产的工艺,针对纳米硒合成原料、合成工艺等做了大量改进,实现纳米硒的快速高效、大规模、一体化合成,实现了工业化规模生产。
目前已经应用到食品及保健品等方面,在富硒农业应用方面直接表现为,生产的富硒农产品含硒量一致性高,能够达到国家关于各类人群定量补硒的要求。
在保健品方面,也做了大量研究,特性包括硒的补充剂、所使用的原料全部为食品来源、良好的生物效应、高稳定性。
结论
纳米硒应用于临床,以下3个方面有待进一步改进及深入研究:
(1)明确纳米硒的作用机理以及寻找准确的作用靶点需要进一步探究。以纳米硒的作用机理及作用靶点为出发点,可望为后续寻找治疗靶点、治疗方向提供更多参考。
(2)在临床上的研究与应用需要更进一步探究。未来需要和更多的医院进行合作,进行大量的临床样本的研究,从而证明纳米硒的普遍的、有效的临床治疗效果,从而进一步推动纳米硒在临床的应用。
(3)基于纳米硒的联合治疗需要进一步的探究。联合治疗是临床上治疗肿瘤的最有效和最常用的方法,因此,开发新的基于纳米硒的复合治疗制剂或者联合治疗方案,能够实现更好的靶向性与治疗效果,为后续纳米硒在临床的大规模推广与应用打下坚实的基础。
本文作者:张泽杭,刘婷,李海伟,桑诚诚,陈义康,陈填烽
作者简介:陈填烽,暨南大学化学与材料学院教授、副院长,广东省纳米化学创新药物工程技术研究中心主任。一直致力于纳米化学创新药物的功能设计与肿瘤诊疗应用研究,担任Journal of Nanobiotechnology副主编、Nano Research等杂志编委。获得国家863计划、国家自然科学基金等项目的资助,入选了万人计划青年拔尖人才及教育部新世纪优秀人才支持计划等。近五年以通讯作者在Cell子刊Matter、Science Advances、JACS、Angew Chem Int Ed等主流杂志发表论文近百篇,其中IF>10有60篇,封面论文38篇,h-index 62,连续两年入选“中国高被引学者”榜单。申报中国专利60项,实现技术成果转化12项。以第一完成人获得2021年高等学校科学研究优秀成果奖技术发明二等奖、2018年中华医学科技奖青年科技奖、2018广东省自然科学二等奖等科技奖励,推动了硒化学在生物医药领域的应用。
论文全文发表于《科技导报》2021年第7期,原标题为《纳米硒的功能设计及其在肿瘤精准治疗中的应用进展》,本文有删减,欢迎订阅查看。

