检测微量元素要多少钱(微量元素检测要抽血吗)

你知道吗?当提到元素周期表中的奇特元素时,铊(Thallium,符号Tl)无疑是其中之一。铊是一种相对稀有的金属元素,它拥有一系列令人着迷的性质和历史背景。从其神秘的发现到危险的毒性,铊元素引人入胜。让我们一起深入探讨这个神秘元素,揭开它的种种谜团,看看它是如何在科学、工业和医学领域中留下深刻印记的。

铊元素虽然具有一些独特的性质,但由于其毒性和稀有性质,它的应用领域相对有限。以下是铊元素在不同领域的详细介绍:
1. 科学研究: 铊在科学研究中具有一定的用途,尤其是在分析化学和光谱学方面。铊化合物常被用作标准物质和参考物质,用于校准仪器和分析实验。铊的特殊光谱特性使其在光谱分析中有所应用。
2. 电子材料: 尽管铊的应用有限,但铊化合物曾在一些电子材料中发挥过作用。例如,铊镉汞(TlCdHg)晶体曾被用于制造红外光电探测器。
3. 治疗: 铊曾经在医学领域中用于治疗一些疾病,如皮肤感染病和肺结核患者的夜间盗汗。然而,由于其极高的毒性,这些用途已经几乎完全被淘汰。
4. 杀鼠剂和杀虫剂: 在过去,硫酸铊曾被广泛用作杀鼠剂和杀虫剂。然而,由于其极高的毒性,多个国家已经禁止了铊化合物在这些用途中的使用。
需要强调的是,铊是一种极其有害的物质,对人类和环境都具有潜在的危险。因此,在任何情况下,使用铊或其化合物都必须谨慎,并遵循严格的安全标准和法规。由于其毒性,铊的实际应用领域已经大幅减少,而更安全的替代品已经取代了它在许多应用中的地位。

铊是元素周期表中的第81号元素,具有一系列独特的物理性质。以下是铊元素的物理性质的详细介绍:
1. 外观: 铊是一种质软、有光泽的金属,通常呈现出银白色到灰色的外观。然而,当它暴露在空气中时,表面会迅速氧化,形成暗灰色的氧化层。
2. 密度: 铊具有相对较高的密度,约为11.85克/立方厘米。这使得它比许多其他常见金属更重。
3. 熔点和沸点: 铊的熔点较低,约为304摄氏度(579华氏度),而沸点约为1,473摄氏度(2,683华氏度)。
4. 电导率: 铊是一种相对差的电导体,其电导率较低。这意味着它不像铜或铝那样能够有效地导电。
5. 磁性: 铊在常规条件下是反磁性的,即不具有永久磁性。
6. 晶体结构: 铊的晶体结构是面心立方(FCC),这是一种常见的金属结构。它在晶体中以紧密堆积的方式排列。
7. 放射性同位素: 铊具有许多放射性同位素,其中最稳定的是铊-203(^203Tl),其半衰期约为22.4年。
8. 热性质: 铊是一种相对不活跃的金属,但它能够与许多非金属元素反应,如卤素和硫。它还可以与酸反应,产生相应的铊盐。
需要注意的是,铊的高毒性使其在现代应用中几乎不再被广泛使用。

1. 电子构型: 铊的电子构型为[Xe] 4f^14 5d^10 6s^2 6p^1,其中最外层电子是一个孤立的p电子。
2. 氧化态: 铊可以形成多个氧化态,包括+1和+3。最常见的氧化态是+1。
3. 反应性: 铊在室温下相对不活跃,但当受热或与氧气等氧化剂接触时,会迅速氧化。铊的化合物通常是带有+1价的铊离子,例如Tl^+。
4. 与硫的反应: 铊与硫(S)反应形成硫化铊(Tl2S),这是一种黑色的化合物。硫化铊是铊元素在实验室中常见的化学反应之一。
5. 与卤素的反应: 铊可以与卤素(氯、溴、碘等)反应,形成相应的卤化铊化合物,如氯化铊(TlCl)、溴化铊(TlBr)和碘化铊(TlI)。
6. 与酸的反应: 铊可以与酸反应,产生相应的铊盐。然而,这些反应通常需要在相对高温下进行。
7. 光谱性质: 铊在光谱学中具有一些独特的性质,其发射光谱被用于分析和测量。
8. 同位素: 铊具有多个同位素,其中最稳定的是铊-203(^203Tl),它是放射性同位素,具有较长的半衰期,可用于一些放射性测量和医学应用。
需要注意的是,铊是一种高度有毒的元素,其化合物具有极高的毒性。因此,在处理铊或其化合物时,必须严格遵循安全措施,以防止接触和污染。铊的毒性性质使其在现代应用中受到限制,而更安全的替代品已经取代了它在许多领域中的使用。

铊是一种有毒元素,其生物特性主要涉及其毒性和影响。以下是铊元素的生物特性的详细介绍:
1. 毒性: 铊是一种极具毒性的元素,对生物体产生严重的毒性作用。它可以以多种方式进入人体,包括吸入、摄入和皮肤接触。铊中毒可能是意外的,但也可能是故意的中毒行为。
2. 生物利用度: 铊可以被生物体吸收和分布到各种组织中,尤其是肝脏、肾脏、神经系统和肌肉组织。铊以其在生物体内的离子形式(通常是Tl^+)存在,与钠(Na^+)具有类似的化学性质,因此可以影响细胞的正常功能。
3. 中毒症状: 铊中毒的症状取决于暴露的程度和时间。早期症状包括恶心、呕吐、腹泻、头痛、腹痛和肌肉痉挛。随着中毒的进一步发展,可能出现更严重的神经系统和心脏问题,如肌无力、共济失调、心律失常和意识丧失。极端的中毒情况可能导致死亡。
4. 诊断: 诊断铊中毒通常基于临床症状、体液样本中的铊浓度以及病史。血液、尿液和头发样本通常用于测量铊的浓度。
5. 治疗: 铊中毒的治疗需要立即采取措施,包括胃洗和使用链合剂(如二巯基丙酸)来促使铊排出体外。支持性治疗,如补液和针对症状的药物,也可能是必要的。
6. 预防: 铊中毒的最佳方法是预防。这包括正确存储和处理含铊的物质,避免接触铊化合物,特别是在实验室和工业环境中采取必要的安全措施,以及遵守相关法规和指南。
需要特别注意的是,由于铊的极高毒性,其在工业和医疗应用中的使用已经受到限制,而更安全的替代品已经被广泛采用。铊中毒是一种严重的医疗紧急情况,应该由专业医务人员进行治疗和管理。

铊在自然界中是一种稀有的元素,通常以微量存在。以下是铊元素在自然界的分布状况的详细介绍:
1. 自然界中的稀有性: 铊是地壳中非常稀有的元素,其自然存在量很低。地壳中铊的平均浓度约为0.5至0.7毫克/千克,这相当于每吨地壳中只有几克铊。
2. 铊的产生方式: 铊通常是通过核衰变的方式产生的,主要是从铋(Bismuth,符号Bi)的放射性衰变中产生。铋-209(^209Bi)是铋的最稳定同位素,它会通过α衰变产生铊-205(^205Tl)。
3. 铊矿石: 尽管铊在地壳中的自然浓度很低,但它可以在一些铋和铅矿石中以微量存在。这些矿石通常包含铋、铅、锡等其他元素。铊通常以微量元素的形式存在于这些矿石中,因此在开采和冶炼过程中通常不是主要目标。
4. 铊的分布: 铊在自然界中的分布是广泛的,但是其自然本底值相对较低。铊可以在土壤、河水、海水、大气中被检测到,但通常是以微量存在。它的分布主要受到地质和地球化学因素的影响,例如地下水流、地壳构造和矿床分布。
5. 人为影响: 铊的自然分布受到人类活动的影响,尤其是与采矿和冶炼有关的活动。铊矿床的开发和铊资源的广泛应用可以导致铊从岩矿石中进入环境介质中,从而增加了铊在环境中的浓度。
铊是地壳中的一种稀有元素,通常以微量存在。它在自然界中的分布受到地质和地球化学因素的影响,并且在人类活动的干预下,铊的浓度可能会在特定地区增加,引发环境和健康方面的担忧。因此,在处理铊和铊相关的活动时,需要采取适当的环保措施和安全措施。

铊元素的开采和提炼过程相对复杂,因为铊通常以微量存在于其他矿石中,而不是作为主要目标矿物。以下是铊元素的开采和提炼过程的详细介绍:
开采铊矿石:
铊通常存在于铋(bismuth)、铅(lead)、锌(zinc)、镉(cadmium)等矿石中。铊矿石的开采通常是与这些其他金属的开采相结合的,因为铊在这些矿石中以微量存在。
1. 勘探: 铊矿床的勘探通常包括地质勘探和地球化学分析,以确定矿床的位置和潜力。
2. 开采: 铊矿石通常通过地下或露天开采方法开采。这取决于矿床的深度和规模。矿石通常需要粉碎和研磨,以便进一步处理。
提炼铊元素:
铊的提炼过程是一项复杂的工程,通常涉及多个步骤,以从矿石中分离出纯铊。
1. 浸出: 矿石通常首先与强酸(通常是硫酸)浸出,以将铊和其他金属溶解成矿液。
2. 分离: 矿液中含有多种金属,包括铊、铋、铅等。通过化学分离方法,可以将这些金属分离开来。最常用的分离方法之一是电解法,其中铊离子被还原成纯铊金属。
3. 精炼: 提炼后的纯铊通常不是非常纯净,还需要进行进一步的精炼。这可以通过化学方法,如萃取、溶解和结晶,以及物理方法,如蒸馏,来实现。
4. 铊的萃取: 铊的提炼中还可以使用有机溶剂来帮助分离和提纯铊。
5. 制备铊化合物: 从提炼的纯铊金属可以制备各种铊化合物,用于不同的应用,例如医学、电子工业和光学。
需要注意的是,由于铊的毒性,提炼和处理铊的工作需要采取极其严格的安全措施,以保护工作人员的健康和环境的安全。在许多国家,对铊的开采和处理都受到法规和监管的监督。

铊元素的常用检测方法主要包括原子吸收光谱法(AAS)、电感耦合等离子体质谱法(ICP-MS)、X射线荧光光谱法(XRF)、原子荧光光谱法(AFS)等。
1. 原子吸收光谱法(AAS):AAS是一种常用的定量分析方法,适用于测定溶液中的铊含量。该方法基于样品中目标元素吸收特定波长的光线时的吸收现象。首先,通过气体燃烧、高温干燥等预处理步骤将样品转化为可测量的形式。然后,向样品中通入与目标元素波长相对应的光线,测量样品吸收的光强度,并与已知浓度的铊标准溶液进行比较来计算样品中铊的含量。
2. 电感耦合等离子体质谱法(ICP-MS):ICP-MS是一种高灵敏度的分析技术,适用于测定液体和固体样品中的铊含量。该方法将样品转化为带电粒子,然后使用质谱仪进行质量分析。ICP-MS具有广泛的检测范围和高分辨率,可以同时测定多个元素的含量。对于铊元素的检测,ICP-MS能够提供非常低的检测限和较高的准确性。
3. X射线荧光光谱法(XRF):XRF是一种非破坏性的分析方法,适用于固体和液体样品中的铊含量测定。该方法通过照射样品表面产生的X射线,测量样品中荧光光谱的特征峰强度来确定其中的元素含量。XRF具有速度快、操作简便的优点,并且能够同时测定多个元素。然而,XRF在低含量铊的分析中可能受到干扰而导致误差较大。
4.电感耦合等离子体发射光谱法(ICP-OES):电感耦合等离子体发射光谱法是一种高灵敏度和高选择性的分析方法,广泛用于多元素分析。它通过将样品雾化并形成等离子体,在光谱仪器中测定铌元素发射的特定波长和强度。
选择合适的检测方法取决于样品性质、所需测定范围和检测精度等因素,并且常常需要校准标准品进行质量控制,确保测定结果的准确性和可靠性。

在元素测量中,原子吸收法具有较高的准确性和灵敏度,为研究元素的化学性质、化合物组成以及含量提供了有效的手段。
接下来,我们使用原子吸收法来测量铊元素的含量。具体的步骤如下:
制备待测样品。将需要测量的样品制备成溶液,一般需要使用混酸进行消解,以便于后续的测量。
选择合适的原子吸收光谱仪。根据待测样品的性质和需要测量的铊元素含量范围,选择合适的原子吸收光谱仪。
调整原子吸收光谱仪的参数。根据待测元素和仪器型号,调整原子吸收光谱仪的参数,包括光源、原子化器、检测器等。
测量铊元素的吸光度。将待测样品放入原子化器中,通过光源发射特定波长的光辐射,待测铊元素会吸收这些光辐射,产生能级跃迁。通过检测器测量铊元素的吸光度。
计算铊元素的含量。根据吸光度和标准曲线,计算出铊元素的含量。
以下是一款仪器测量铊元素用到的具体参数。

铊(Tl)
标准物:硝酸铊TlNO3(99.99%)。
方法:准确称取1.303g TlNO3,溶于20mL1%的HNO3中,用水准确定容至1L,此溶液中Tl的浓度为1000μg/mL。避光保存于聚乙烯瓶中。
火焰类型:空气-乙炔,贫燃焰。
分析参数:
波长(nm)276.8
光谱带宽(nm)0.4
滤波系数0.3
推荐灯电流(mA)3
负高压(v)348.5
燃烧头高度(mm)10
积分时间(S)3
空气压力及流量(MPa,mL/min)0.20
乙炔压力及流量(MPa,mL/min)0.05,1500
线性范围(μg/mL)0.1146~20
线性相关系数0.999
特征浓度(μg/mL)0.140
检出限(μg/mL)0.038
RSD(%)0.48
计算方式连续法
溶液酸度0.5% HNO3
测量表格:

校准曲线:
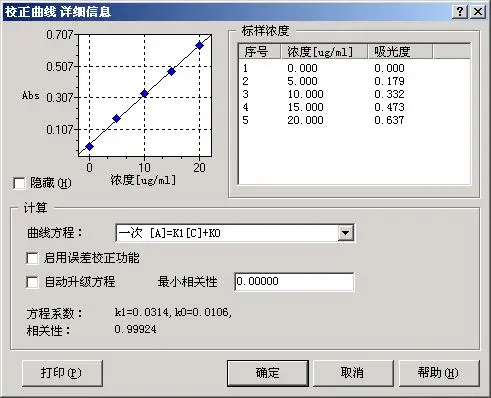
干扰:
在空气-乙炔火焰中没有干扰,此元素及其溶液对人体有毒害作用,小心处理。377.6nm谱线可测定高含量的铊。
实际工作中需要根据现场具体需要选择适合的测量方法。这些方法在实验室和工业中广泛应用于铊元素的分析和检测。
#日常生活中的理化检测分析#

