膜性肾炎可以补硒吗(慢性肾炎可以吃硒酵母片吗)
鉴别继发性IgAN无捷径,知识储备很重要!
随着IgA肾病(IgAN)在我国流行态势增加,临床上也愈加重视这一疾病。这种以肾小球系膜区IgA异常沉积为特点的肾病虽然被许多同行所熟知,但对于病因的鉴别诊断缺乏关注。通常“IgA肾病”都与“原发性肾病”挂钩,然而对于存在系统性疾病的患者而言,同时出现IgA免疫复合介导肾脏损伤之后,即定义为“继发性IgA肾病”。
对原发和继发的IgA肾病进行病因鉴别,关系到患者治疗响应和预后等重要方面。在中国医师协会肾脏内科医师分会2021年学会年会暨中国工程院医药卫生学部肾脏病前沿会议上,复旦大学附属中山医院丁小强教授带来了精彩的相关分享。
横看成岭侧成峰:看似一样,实则不同!
我国IgAN诊治指南指出,IgAN诊断首要重点为明确是否存在继发性疾病。继发性IgAN与原发性IgAN在组织表现上并无显著差异,因此鉴别继发性IgAN的基础是严谨的临床分析、详尽的病史采集和完善的体格检查,在此基础上全面排查继发性病因,关注病程中症状、体征和实验室检查的变化,才能减少继发性IgAN的误诊和漏诊。
IgAN是基于组织免疫病理的诊断,而形态学表现相似的背后往往隐藏着巨大的差异。
从发病机制而言,原发性IgAN的发病主要有4个过程:
①IgA1分子糖基化异常;
②半乳糖缺陷IgA1分子可形成多聚体,或与抗异常IgA1的IgG抗体结合,形成循环免疫复合物;
③沉积于肾小球系膜区;
④导致炎症反应和系膜损伤。
而继发性IgAN的发病机制则有所不同,主要有3方面引起了人们的关注:
①遗传与环境的诱因;
②肝脏疾病与粘膜炎症的患者常见IgAN;
③循环IgA免疫复合物和系膜IgA沉积中发现许多饮食和微生物抗原。
正常的IgA免疫应答包括3个步骤,即暴露于抗原、B细胞在T细胞的帮助下合成IgA、清除循环中含有IgA的免疫复合物。一旦免疫应答失调,血清中出现过量致病性IgA时,致病性IgA的粘膜表型则会造成负面影响,并且这种致病性IgA与占据系统免疫部位的黏液刺激有关。
也正因于此,IgA免疫系统与继发性IgAN发展成相关疾病之间也存在相互的关系(图1),总而言之:导致继发性IgAN的病因与IgA合成增多以及清除减少有关。
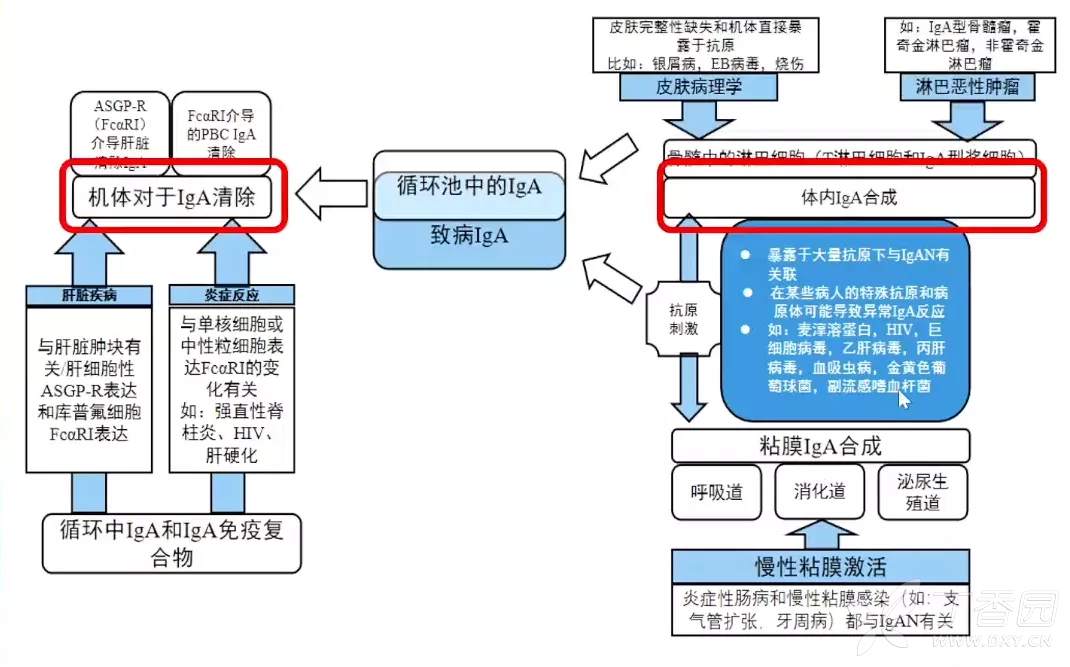
图1.IgA免疫系统与继发性IgAN发展成相关疾病之间的相互关系
远近高低各不同:这么多种继发性IgAN的病因,如何鉴别?
可见,完全鉴别原发性和继发性IgAN需要大量的临床知识储备才能够做到抽丝剥茧、真相大白。目前,已知可以导致IgAN的继发性病因纷繁多样,如表1所示。
表1.常见导致继发性IgAN的病因

在初步对继发性IgAN病因进行储备后,临床上遇到需要鉴别的IgAN患者时,医生应当仔细询问病史,包括肾脏以外的系统性症状、近期感染史、职业和既往史等,并对包括皮肤、关节、淋巴结以及肝脾在内的组织器官进行全面的体格检查。
辅助检查方面,除了关注血象、免疫学结果(自身抗体、补体、免疫球蛋白、冷球蛋白、类风湿因子、免疫固定电泳)以外,还需要关注肝炎以及其他肝炎性标志物,如结核感染T细胞斑点试验等。必要时,还应进行甲状腺功能以及影像学等检查。
而在这一切的尽头,肾活检病理也很重要,根据病理表现决策是否需要排查继发性因素、关注特定抗原和评估抗体免疫荧光染色等。
不识庐山真面目:继发性IgAN到底还有多少秘密?
目前为止,人们并没有全部了解许多疾病,包括继发性IgAN。在2020年的一份案例报告中[1],作者发现了半乳糖缺乏性IgA1特异性地参与了原发性IgAN地发病机制,通过免疫荧光染色发现了半乳糖缺乏IgA1的特异性单克隆抗体(KM55),KM55在原发性IgAN中显示出特异性阳性,或可作为鉴别原发性与继发性IgAN的标志物。
有研究提示[2],Gd-IgA1单克隆抗体或可作为鉴别的重要手段,但该结论尚待进一步验证。然而鉴别继发性IgAN的新手段依旧有限,因此仍需掌握临床常见的继发性IgAN与原发性IgAN的鉴别要点。
紫癜性肾炎
在继发性IgAN中,过敏性紫癜导致的紫癜性肾炎是继发性IgAN的最主要类型(儿童尤甚)。紫癜性肾炎与原发性IgAN的光镜表现类似,但是活动性病变较原发性IgAN更为常见,如系膜增生节段加重突出、出现更多的新月体、袢坏死等,罕见表现甚至可见膜增生性肾炎伴基底膜双规轨形成。而从临床表现上,原发性IgAN无皮肤表现,紫癜性肾炎则有特征性的紫癜性皮疹,不过须谨记的是皮肤紫癜往往出现在肾性表现或其他内脏紫癜之后。
感染相关IgAN
感染相关IgAN容易被误诊为原发性IgAN或急性感染后肾小球肾炎,常见于老年人和糖尿病患者,发病前常有感染史(内脏/皮肤/关节等),一般潜伏2-4周。此类患者病原检测一般可见链球菌、皮肤以及深部金葡菌感染,临床可见血尿、蛋白尿、急性肾损伤以及低补体血症和高血压。
与典型的急性感染后肾小球肾炎相比,感染相关IgAN的临床病程相似,但病理表现为IgA沉积的弥漫性毛细血管内和/或系膜增生性肾小球肾炎,并可伴有C3、Ig沉积,IgA主要沉积于毛细血管壁上,电镜下可见特征性的上皮下“驼峰状”致密沉积。
此类继发性IgAN需要强调病毒性肝炎继发性IgAN,虽然机制不明确,但是诊断依据相对清晰:血清肝炎标志物阳性、肾脏受累、肾活检出IgA沉积外可见HBV或HCV抗原以及除外其他继发性病因。
风湿免疫系统疾病继发IgAN
许多风湿免疫系统疾病均可累及肾脏,容易出现不同程度的血尿、蛋白尿和肾损害,此类患者肾穿刺活检可见IgAN相似的病理表现(表2)。鉴别时可见此类继发性IgAN患者有多系统受累,一些特异抗体呈阳性也具有提示意义。
表2.常见风湿免疫疾病的肾活检病理特点
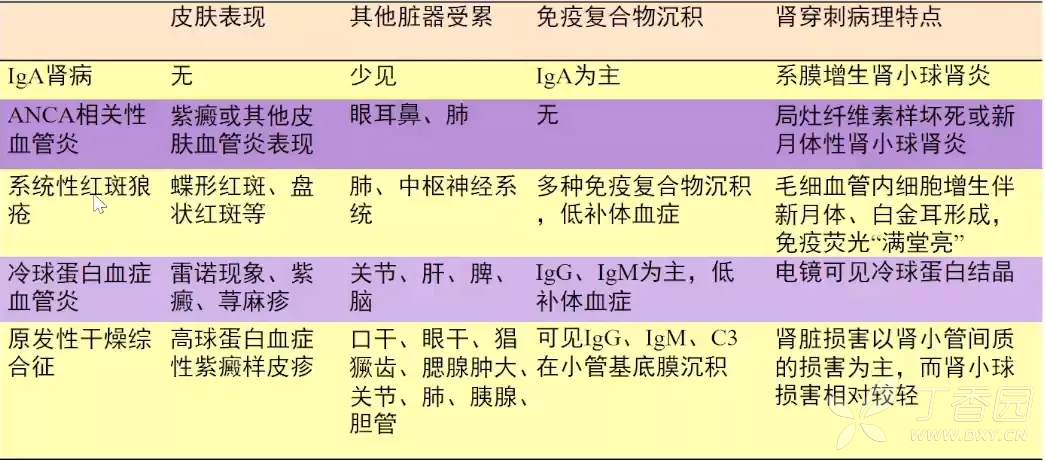
粘膜炎症性疾病继发IgAN
溃疡性结肠炎和克罗恩病与IgAN相关的报道近年来增多,有研究表明炎症性肠病合并的肾损害中,IgAN是最常见的一种,并且可以在炎症性肠病活动或缓解后都可以出现[3]。此外,乳糜泻也容易继发IgAN,但这种继发性IgAN免疫荧光通常没有C3沉积。
肝脏疾病继发IgAN
在肝移植病例中,9%-25%的患者肾活检可见IgAN。其发病机制可能与免疫复合物或多聚IgA生成过多,同时肝脏清除能力下降有关。肝病相关肾损伤的肾脏病理类型复杂,肾小球损伤以IgAN最为常见,而新月体形成和肾小管间质病变比例高,免疫荧光染色可见肾小球系膜区IgA阳性,偶尔也可见IgG和IgM阳性。此类患者肾脏损害症状轻且发病晚,因此可对肝硬化病史的患者密切随访尿检和肾功能变化,必要时以肾脏穿刺活检进行临床指导。
肿瘤继发IgAN
目前可见个案报道中消化道肿瘤、肺癌和淋巴癌继发IgAN,大多数患者表现为镜下血尿,偶尔肉眼血尿、蛋白尿和肾功能不全。虽然肿瘤继发IgAN表现隐匿,无典型症状,但是建议全面筛查。然而,确诊肿瘤继发IgAN后,治疗应当以原发病为主、为先。
总结
继发性IgAN常见病因包括过敏性紫癜、慢性感染、自身免疫性疾病、慢性肝病、粘膜炎症以及肿瘤等,鉴别诊断应当从详细病史、全面体检、针对性检查以及最重要的肾穿刺病理几个主要方面入手。目前新近研究进展认为半乳糖缺乏IgA1特异性单克隆抗体KM55或可作为鉴别原、继发性IgAN的重要标志物,但这一结论仍需进一步证实。
参考文献:
[1]Lee M, Suzuki H, Kato R, et al. Renal pathological analysis using galactose-deficient IgA1-specific monoclonal antibody is a strong tool for differentiation of primary IgA nephropathy from secondary IgA nephropathy[J]. CEN Case Reports, 2021, 10(1): 17-22.
[2]Suzuki H, Yasutake J, Makita Y, et al. IgA nephropathy and IgA vasculitis with nephritis have a shared feature involving galactose-deficient IgA1-oriented pathogenesis[J]. Kidney international, 2018, 93(3): 700-705.
[3]Ambruzs J M, Walker P D, Larsen C P. The histopathologic spectrum of kidney biopsies in patients with inflammatory bowel disease[J]. Clinical Journal of the American Society of Nephrology, 2014, 9(2): 265-270.
本文首发:医学界肾病频道
继续阅读
- 暂无推荐

