孕妇补硒补锌的作用(孕妇补锌有什么用)

Introduction
你是否常感到头晕气短,机体无力,身体疲倦?你是否皮肤苍白,出现勺状指甲?那很有可能是缺铁性贫血!缺铁性贫血作为一种发病率较高的营养缺乏性疾病,据WHO统计,全球约有80%的人口缺铁,我国则约有10%的人患有缺铁性贫血。缺铁性贫血是由于体内铁供需失衡,导致体内贮存铁耗尽,血红蛋白的合成减少,以致红细胞数量减少从而引起氧代谢障碍、机体代谢紊乱引发的。而铁作为人体所必需的微量元素,会参与体内氧的运输、细胞呼吸、核酸合成等多种生理活动,当人体铁的需求增加(如孕妇、婴幼儿、青少年),铁摄入或吸收障碍(如素食主义者、胃肠道疾病患者),铁丢失过多(如一些慢性失血患者)时就容易引起铁供需失衡。而对于缺铁性贫血的治疗目前多采用口服补铁剂的方式,但是传统的补铁剂如硫酸亚铁、富马酸亚铁等,虽然价格便宜、疗效也很好,但是会引起严重的胃肠道刺激,导致患者难以坚持治疗。因此,开发一款新型高效且安全的补铁剂迫在眉睫。
多糖铁复合物,以大分子多糖为配体和三价铁离子Fe(Ⅲ)络合而成,含有人体必需的铁离子和促进铁离子吸收的有机成分,不受膳食因素影响,吸收率高且对胃肠道损害小,同时不仅有很好的补铁功效还兼具其他的生理活性,如抗氧化、免疫调节、抗菌、抗肿瘤等等。而食用菌营养价值高且具备多种生物活性物质,以食用菌多糖作为配体制备多糖铁复合物有着广阔的市场前景和工业价值。
金针菇(Flammulina velutipes)又名冬菇、朴菇、毛柄金钱菌等,作为我国五大食用菌品种之一,价廉易得,含有丰富的碳酸化合物、蛋白质及多种维生素和矿物质元素,具有很高的食用及药用价值。多糖作为其主要的功效成分之一,具有抗氧化、抗衰老、抗病毒、抗肿瘤、提高机体免疫力等多种生理性功效,而以其为原料来制备一种新型的多糖铁复合物可谓潜力十足。近年来,中国药科大学陈贵堂教授课题组已经在金针菇多糖铁复合物的功效研究方面取得了一系列的成果,前期研究发现金针菇多糖铁复合物(FVP1-Fe(III))相较硫酸亚铁在体外消化道中能保持较好的溶解度和稳定性(Int J Biol Macromol, 2019, 132, 801-810)。在此基础上,本文建立体外细胞模型和缺铁性贫血动物模型,研究其在体外的吸收转运机制及体内的补铁功效,为新型多糖铁复合物的开发和应用提供参考。该成果发表在最新一期的《Food Science and Human Wellness》上,中国药科大学硕士研究生石晨莹为文章的第一作者,陈贵堂教授为文章的通讯作者,该系列研究成果是在国家重点研发计划项目(2017YFD0400203)资助下完成的。
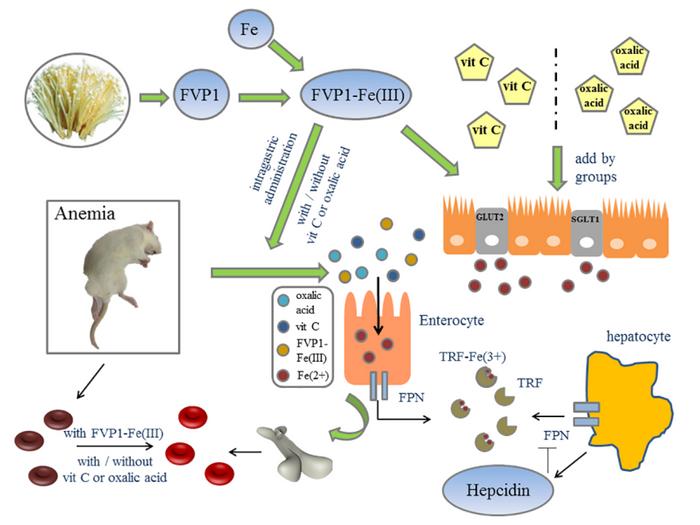
Results and Discussion
FVP1-Fe(III)在体外Caco-2细胞模型中的吸收转运机制
首先验证金针菇多糖铁复合物FVP1-Fe(III)在体外的安全性,利用CCK8法检测发现FVP1-Fe(III)在5~800 μg/mL的浓度下对Caco-2细胞没有毒性(图1A)。接着,建立Caco-2细胞单层模型,通过双向转运筛选合适浓度的FVP1-Fe(III)(5,50,500 μg/mL)进行后续实验,如图1B-C和表1所示,5 μg/mL的FVP1-Fe(III)的转运量显著高于硫酸亚铁且相较于其他浓度的FVP1-Fe(III)的表观渗透系数更高,更有利于铁的传递。然后添加摄取抑制剂、外排抑制剂及膳食影响因素并通过测定FVP1-Fe(III)的转运量来研究FVP1-Fe(III)体外的吸收转运机制,根据图1D所示的结果可知FVP1-Fe(III)的摄取不通过细胞旁路途径及经磷酸肌醇3-激酶位点抑制的胞吞途径,而是通过GLUT2和SGLT1两种葡萄糖转运载体且GLUT2发挥主要作用,而FVP1-Fe(III)的外排是通过MRP-2转运蛋白而非P-gp。此外,维生素C会促进FVP1-Fe(III)在体外的吸收。最后,通过实时荧光定量PCR检测经FVP1-Fe(III)处理后的Caco-2细胞相关转运蛋白的表达情况,再次验证了FVP1-Fe(III)的吸收转运机制(图1E)。总之,FVP1-Fe(III)在体外的吸收转运主要是由SGLT1和GLUT2参与的,且GLUT2起主要作用,而其外排则是由MRP-2介导的。
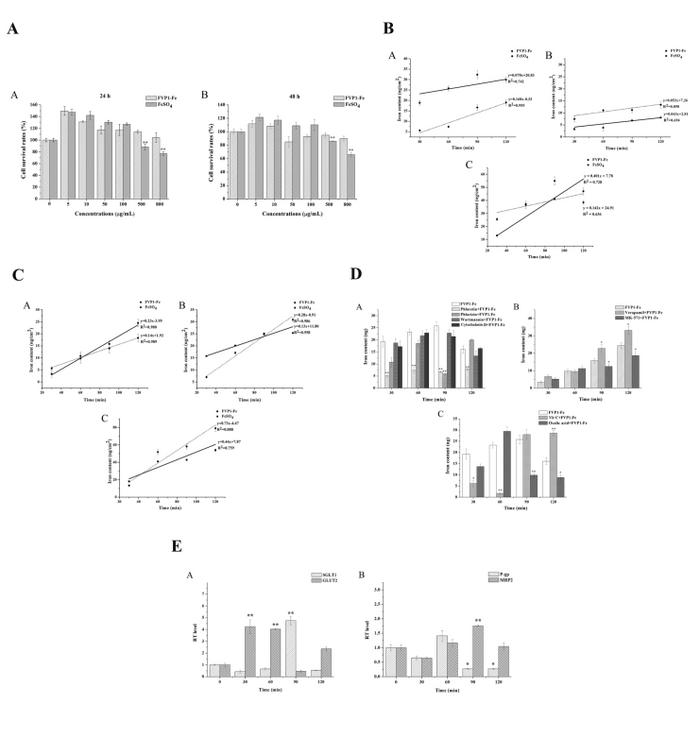
图
1(A) Caco-2细胞存活率检测; (B)不同浓度的FVP1-Fe(III)从AP转运到BL侧的量; (C)不同浓度的FVP1-Fe(III)从BL转运到AP侧的量;(D)摄取、外排抑制剂和膳食影响因素对FVP1-Fe(III)的转运的影响;(E)相关转运蛋白的表达情况
表1 不同浓度FVP1-Fe(III)的表观渗透系数

FVP1-Fe(III)在体内改善缺铁性贫血
在研究FVP1-Fe(III)的体外吸收转运机制及传递铁的能力后,为进一步研究FVP1-Fe(III)的补铁功效,本研究建立了缺铁性贫血大鼠模型。如图2A所示,FVP1-Fe(III)可以改善由缺铁性贫血造成的体重下降甚至可以增加大鼠体重。根据表2所示结果可知,FVP1-Fe(III)可以恢复缺铁性贫血引起的脏器指数改变,且相比于会引起肾脏毒性的硫酸亚铁更安全。如图2B所示,FVP1-Fe(III)可以改善缺铁性贫血造成的肝脏损伤。如表3和表4所示,中剂量的FVP1-Fe(III)可以更好地改善由缺铁性贫血引起的红系参数和铁状态指标的改变且维生素C可以促进FVP1-Fe(III)的吸收帮助FVP1-Fe(III)更好地发挥作用。此外,FVP1-Fe(III)不仅可以改善缺铁性贫血造成的肠道菌群紊乱还可以提高有益菌丰度从而改善肠道环境(图2C)。最后,还利用实时荧光定量PCR测定体内hepcidin的表达情况从而研究FVP1-Fe(III)的补铁机制,如图2D所示,发现FVP1-Fe(III)通过抑制肝脏中hepcidin的表达来发挥补铁功效。

图2(A)大鼠体重随FVP1-Fe(III)给药时间的变化;(B)肝脏切片的观察;(C)大鼠肠道菌群的改变;(D)大鼠hepcidin表达水平的变化
表2 大鼠脏器指数的改变

表3大鼠红系参数的改变
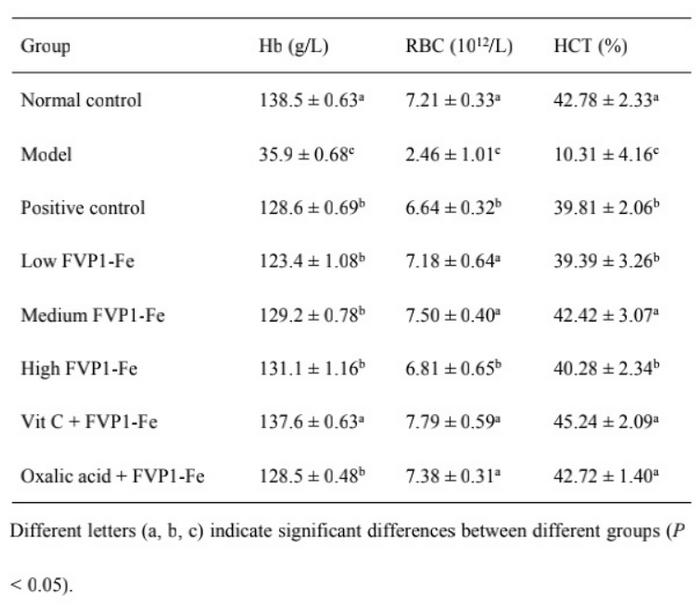
表4大鼠铁状态指标的改变
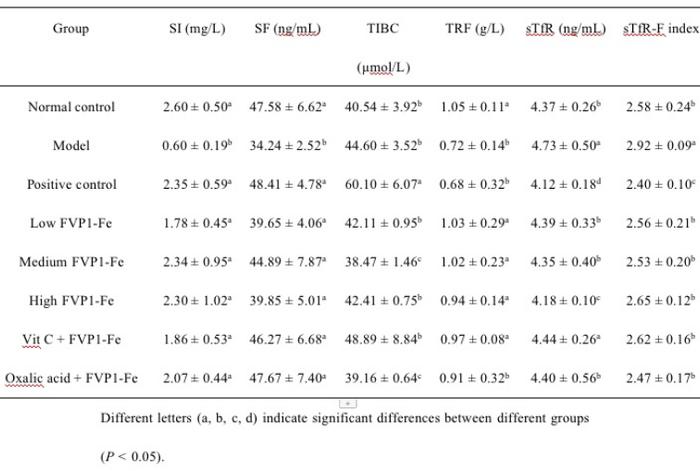
Conclusion
本文研究了金针菇多糖铁复合物FVP1-Fe(III)在体外的吸收转运机制及体内的补铁功效。FVP1-Fe(III)在Caco-2细胞中的摄取主要由GLUT2和SGLT1(两种己糖转运体)介导,外排主要由MRP-2介导。此外,FVP1-Fe(III)治疗可改善缺铁性贫血大鼠的生长、红系参数、铁状态指标和肝组织形态,并调节肠道微生物群,以改善缺铁性贫血引起的肠道微生物群失调并改善肠道健康。FVP1-Fe(III)与维生素C一起使用还可以发挥更好的效果。此外,FVP1-Fe(III)通过抑制hepcidin表达来调节体内铁水平,这是FVP1-Fe(III)在体内的基本机制。重要的是,与传统补铁剂硫酸亚铁相比,FVP1-Fe(III)在吸收和利用方面更有效也更安全。因此,FVP1-Fe(III)复合物非常有潜力成为一种新型的铁补充剂。
第一作者

石晨莹,硕士研究生,现就读于中国药科大学工学院,研究方向为营养与功能食品。
通信作者

陈贵堂,中国药科大学工学院/国家中药材加工研发专业中心教授,博士生导师。毕业于中国农业大学食品科学与营养工程学院,获工学博士学位,美国罗格斯大学食品科学系访问学者,入选江苏省“双创计划”科技副总项目。主要研究食品及药食同源品等材料中生物活性物质的药理活性与保健作用机理,尤其是功能成分与人类慢性疾病的关系,同时采用先进的物理、化学和生物学技术,研究功能性成分的高效分离和富集、活性保持和增效,为医药、保健食品开发提供各种功能因子。完成了国家重点研发计划项目子课题、国家自然科学基金、江苏省自然科学基金等项目10余项,在国内外期刊上发表科研论文90多篇,获授权专利10余件。
Flammulina velutipespolysaccharide-iron(III) complex used to treat iron deficiency anemia after being absorbed via GLUT2 and SGLT1 transporters
Chenying Shi
a,1
, Chen Cheng
a,1
, Xiaotong Lin
, Yanfang Qian
, Yufeng Du
, Guitang Chen
a,
Department of Food Nutrition and Safety/National R&D Center for Chinese Herbal, Medicine Processing, China Pharmaceutical University, Nanjing 211198, China
College of Pharmacy, China Pharmaceutical University, Nanjing 211198, China
*Corresponding author.
Abstract
Iron deficiency anemia(IDA) is a common nutritional problem, but traditionaliron supplementscause many adverse reactions。 Thus, the development of a novel iron supplement might be significant for the treatment of IDA。 This study aimed to study the transport mechanism ofpolysaccharide-iron complex (FVP1-Fe(III)) in Caco-2 cells and the therapeutic effect on IDA rats, as well as the influence ongut microbiotaFlammulina velutipesin vivo。 These results showed thatin vitro, the uptake of FVP1-Fe(III) was mediated by sodium-dependent glucose transporter-1 (SGLT1) and facilitated glucose transporter-2 (GLUT2) and GLUT2 played a dominant function。
The multidrug resistance-associated protein-2 (MRP-2) was involved in the efflux of FVP1-Fe(III) across the Caco-2 cells。In vivo, FVP1-Fe(III) had a better restorative effect on blood parameters and iron status indicators in rats with IDA as compared with FeSO4and exerted this effect by downregulating the expression ofhepcidin。 FVP1-Fe(III) could also regulate gut microbiotadysbiosisiniron deficiencyrats by returning the relative abundance of gut microbiota to the normal level。 Besides, as a dietary factor,vitamin C(vit C) could enhance the therapeutic effect of FVP1-Fe(III)。 These present findings showed that FVP1-Fe(III) could be exploited as a novel iron supplement to treat IDA。
Reference:
SHI C Y, CHENG C, LIN X T, et al.Flammulina velutipespolysaccharide-iron(III) complex used to treat iron deficiency anemia after being absorbed via GLUT2 and SGLT1 transporters[J]. Food Science and Human Wellness, 2023, 12(5): 1828-1840. DOI:10.1016/j.fshw.2023.02.047.

