锌硒宝壳聚糖凝胶(锌硒宝压片糖果)
壳聚糖
一 甲壳质和壳聚糖
1.1 甲壳素
甲壳素,又名甲壳质、几丁质,化学名称(1,4)-2-乙酰氨基-2-脱氧-β-D-葡聚糖。是一种天然高分子多糖[1],大量存在于海洋节肢动物,如虾、蟹的甲壳之中,也存在于菌类、昆虫类、藻类细胞膜和高等植物的细胞壁中[2],分布极其广泛。甲壳素在自然界每年的生物合成量仅次于纤维素,是地球上第2大可再生资源。
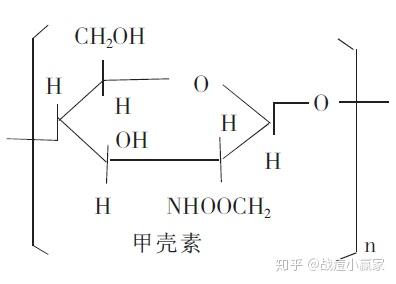
甲壳质最早在1811年由法国科学家Braconot从霉菌中发现,1859年法国人C.Rouget用浓KOH处理甲壳质,出现了壳聚糖。直到20世纪50年代,才对甲壳质的化学结构、性质和制备方法有了较深透的了解。
甲壳质资源丰富,制法简单,价格低廉,又因其具有良好的化学物理性质:能拉丝、成膜制粒,能通过化学改良物化特性;能和多种物质(如胆固醇、脂肪、重金属、蛋白质、肿瘤细胞等)结合;无毒且有生物相容性,因此可用于许多领域。
1.2 壳聚糖
壳聚糖(Chitosan),又名:脱乙酰甲壳质、可溶性甲壳素、聚氨基葡萄糖,化学名称为:β-(1,4) -2-氨基-2-脱氧-D-葡聚糖,是由甲壳质经脱乙酰作用,脱去C2上的乙酰基而得到。
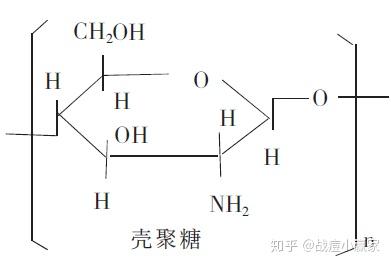
壳聚糖呈白色或灰白色,略有珍珠光泽,半透明无定形固体,约在185℃分解,不溶于水和稀碱溶液,可溶于稀有机酸和部分无机酸(盐酸),但不溶于稀硫酸、稀硝酸、稀磷酸、草酸等。
壳聚糖同时含有羟基和氨基,二者可以通过酰化、羧基化、羟基化、氰化、醚化、烷化、酯化、醛亚胺化、叠氮化、成盐、螯合、水解、氧化、卤化、接枝与交联等反应生成各种不同结构和不同性能的衍生物。
1.3 脱乙酰反应
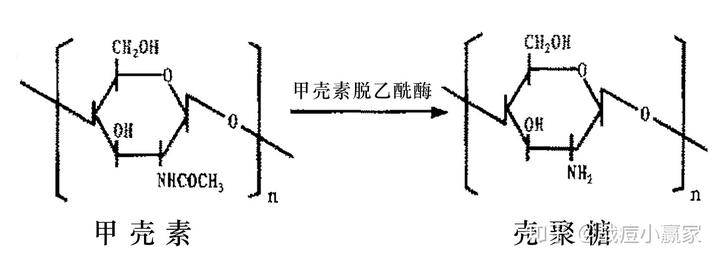
甲壳质经过脱乙酰基即可制取壳聚糖,常用质量分数为45%-50%氢氧化钠溶液浸泡甲壳质并加热至105℃,保温2h,水洗至中性,抽滤,干燥即可得到白色略带珍珠光泽的壳聚糖。其中碱液浓度、反应温度及反应时间是影响壳聚糖的性能指标(脱乙酰度和相对分子量)的主要因素。另外不同原料( 螯虾壳、海蟹壳、对虾壳、河虾壳和蚕蛹)用同一方法在相同条件下,制备壳聚糖,收率分别为13.6%、12.3%、10.5%、8.70%、1.8%[3],可见螯虾壳和海蟹壳是首选原料。此外,还可用酶法[4]、微波法[5,6]制备壳聚糖。
另外还可以利用微生物的菌体结合生物技术提取壳聚糖[7],如Mucor rouxii[8]、Absidia butleri、Abesidiacorrulea[9]、蓝色梨头菌[10]、柠檬酸废菌体[11]等;该方法不受原料季节性影响,发展前景看好。
二、研究发展历史
1811年,法国科学家H. Braconnot从动物的甲壳中提取到了甲壳素 。
1859年,法国人Rouget将甲壳素放在浓KOH溶液中煮沸,洗净后可溶于有机酸,便得到了壳聚糖 。
1934年,在美国才首次出现了关于制备壳聚糖及相关物质的专利,并于1941年成功制备壳聚糖人造皮肤和手术缝合线 。
20世纪90年代,壳聚糖的应用和生产达到了高潮——全球壳聚糖的年产量数万吨。
目前提纯工艺最好的壳聚糖成品是法国南部布列塔尼大学海洋生物研究所研制,其通过先进生物工程技术,将甲壳素里面的乙酰基逐步脱掉达到纯度高于普通级别脱乙酰度55%,目前全球壳聚糖药用原材料70%来自布列塔尼地区,其出品的医药级壳聚糖是脱乙酰度95%以上的成品。脱乙酰纯度达到95%以上的壳聚糖纯度较高,有极强的活性,主要用于医药领域,对伤口的愈合有着快速的修复,并有抑菌性预防伤口感染,高纯度壳聚糖的多效作用已经越来越被外科医生所追捧。
三、壳聚糖的性质
壳聚糖是天然高分子中少有的碱性多糖,不溶于水和有机溶剂,可溶于Ph
由于壳聚糖的生物可降解性、低毒、良好的生物相容性使其广泛应用于生物医药和制剂[14]。研究发现,壳聚糖具有抗酸、抗溃疡,促进伤口愈合等性质;作为各种剂型的辅料,壳聚糖既可用作片剂崩解剂、黏合剂,也可制成颗粒剂、眼用膜剂等。壳聚糖能够成为新型的纳米药物载体,其特有的黏膜黏附性是主要因素之一。
壳聚糖是性能优良的天然黏膜黏着剂,常用于多肽类药物的黏膜给药。以壳聚糖制成的纳米载体可以延长药物在吸收位置的保留时间,达到控释目的[15]。生物黏膜表面的类脂层荷负电,易与带正电荷的壳聚糖粒子发生静电吸附,增强了大分子药物透过黏膜吸收的能力。经过体内实验研究,van der I_nbben等[16]认为以壳聚糖纳米粒包裹的抗原如卵清蛋白、白喉类毒素、破伤风类毒素等,能够减少胃肠道酶降解而被肠淋巴组织(GAIT)的Peyer’s区充分摄取,这为壳聚糖纳米载体应用于疫苗的口服给药提供重要依据;另外在抗原的鼻疫苗研究中,发现以壳聚糖为载体能够显著增强黏膜和系统的免疫反应,说明壳聚糖也适于疫苗的鼻黏膜给药。
将壳聚糖应用于纳米载体的研究,是20世纪90年代末逐渐发展起来的新兴研究领域。研究人员对壳聚糖纳米载体的制备技术及应用前景展开了广泛而深入的探索,并取得了阶段性、突破性的进展,这为将来更深入系统的研究提供了重要的理论与技术支持。
四、壳聚糖应用
4.1 在医药卫生方面的应用
在医药学领域,甲壳素或壳聚糖及其衍生物还可以提高黏膜的通透性,可以作为靶向载体,可以用于制备生物材料等。如Kotze-AF实验发现,三甲基壳聚糖四聚体的盐酸盐可提高消化道黏膜通透性[17];以壳聚糖制成胶囊包裹R68070(一种新型的血栓烷合成酶抑制剂)用来治疗溃疡性结肠炎,可避免药物在酸性环境中的破坏和吸收,使其到达病变结肠部位(pH约为7.4),取得良好的治疗效果[18];以壳聚糖制成的生物管用于桥接缺损神经,可以抑制成纤维细胞的生长,进而防止神经瘤的形成,为轴突的生长创造有利的微环境;在磷酸钙骨水泥中加入壳聚糖作为配料,可以提高骨水泥的内聚力,防止其在体内降解,并具有良好的组织相容性[19];甲壳素或壳聚糖及其衍生物也可用于酶的固定化方面;可作为骨缺损支架材料,还可制备组织工程所需的支架材料,用于人工骨等人工器官的体外培养;各种微球形壳聚糖胺基衍生物可有效地吸附牛血清蛋白,为新型功能吸附剂[20]。
由于甲壳质、壳聚糖具有与人体良好的生物相溶性和生物可降解性,其降解产物可被人体吸收,在体内不蓄积,无免疫原性,在医药卫生方面有着广泛的应用[21]。在2008年4月的美军战术区战伤救治的变革的(TCCC)指南中,美国军方特别批准使用壳聚糖敷料作为止血剂[22]。
4.1.1 医用纤维和膜材料
用甲壳质、壳聚糖纤维制成的手术缝合线已应用于临床.与传统的羊肠线相比,用壳聚糖制成的吸收型外科手术缝合线材料柔软,易打结,机械强度高,易被机体吸收,同时不改变皮肤胶原蛋白中羟脯氨酸含量,无炎症反应,还可用常规方法消毒,增加伤口的抗张强度,加速伤口愈合。
用壳聚糖制成的医用纤维膜具有均匀、透明、手感好、柔软、良好的透气性、吸水性和杀菌性等优点。
4.1.2 药物载体
用壳聚糖作为药物载体可以稳定药物中的成分,促进药物吸收,延缓或控制药物的溶解速度,帮助药物达到靶器官,并且抗酸、抗溃疡,防止药物对胃的刺激。
4.1.3 凝血作用
包扎用纱布经甲壳质粉末或壳聚糖溶液处理后包扎伤口,能立即止血,并有消炎作用,伤口愈合速度提高75%.伤口长好后纱布不粘连,甚至不留痕迹。用壳聚糖制成止血海绵,能够立即止血,临床效果非常好。
4.1.4 抗肿瘤作用
甲壳质能选择性地凝聚白血病的L 1210细胞、Ehrlich 腹水癌细胞,对正常的红血球骨髓细胞无影响。试验证明,将180肉瘤植入dd 小鼠体内,7d 后以静脉注射的方式将两种甲壳质(Hexa-N-acctylchitohexaose 和Chitohexaose)打入小鼠体内,连续注射3d(100mg(kg·d)),结果可明显抑制肿瘤生长,抑制率分别达到85%和93%。
4.1.5 增强免疫力
壳聚糖能有效地增加巨噬细胞的吞噬功能和水解酶的活性,通过增强机体非特异性免疫系统的功能而抑制肿瘤生长。巨噬细胞激活后,除了本身的吞噬杀灭肿瘤细胞等功能增强外,又能分泌多种免疫因子调节其他细胞免疫与体液免疫。此外,壳聚糖还可显著促进脾脏细胞生成抗体的能力。
4.1.6 降低脂肪和胆固醇
通过人体观察显示:摄食壳聚糖能有效降低血清胆固醇。8位健康男性成人,摄食壳聚糖3-6g/d,两周后其总血清胆固醇下降(由188mg/dl降为177mg/dl)并增加高密度胆固醇(HDL-cholesteral,由51mg/dl增至56mg/dl)。同时可降低胃酸,抑制溃疡,具有健胃的作用。
4.1.7其他方面
可用于治疗过敏性皮炎,预防龋齿和牙周炎,除去和减轻口臭,还可降低肾病患者血清胆固醇、尿素及肌酸水平。此外,还可制成各种人工器官,如:人工肝脏、人工肾、人造骨、人造血管等。
4.2. 在头发方面的应用
4.2.1. 壳聚糖在洗发水中的应用
洗发水的主要成分是表面活性剂,若能合理的添加少量的壳聚糖,就能减少或代替洗发香波中添加的护发、养发、滋润等成分,而使产品在使用过程中产生多重作用,即有洗发、护发及抗静电作用,同时又具有滋养定型之功效,使洗后的头发各种性能大为改观。
4.2.2.壳聚糖在固发剂中的应用
壳聚糖作为发型固定剂的原料与通常的阳离子、阴离子和非离子型树脂制成的普通固发剂相比,在头发表面形成的薄膜其硬度适中,且不发粘,特别是在湿度较大和出汗的情况下仍能保持原来的硬度而不发粘。普通的固发剂在头发疏理或揉擦时,具有明显的静电作用,很难长时间保持发型。而由壳聚糖配制的固发剂,具有抗静电作用,少量使用就能保持发型。特别是对某些敏感性皮肤的人,使用壳聚糖为原料的固发剂可以减少或避免皮肤过敏或灼烧感的发生。
4.3 在化妆品中的应用
利用壳聚糖的保湿性、润湿性、成膜性、抗静电作用、毛发柔软和保护作用,以及对皮肤无刺激、无毒等特性在化妆品中具有广泛的应用。
研究证明,皮下水分的散失是人的皮肤衰老的主要原因之一,而壳聚糖具有优良的保湿性和润湿性。与某些化学合成的保湿剂相比较,它无毒、无害、对皮肤和眼粘膜无刺激,不存在接触过敏的问题,而且价格便宜,因此将其应用于护肤品中,使产品具有优良的性能,并能全部或部分代替通常所用的保湿及润湿成分。
裂解后的寡聚葡萄糖胺和葡萄糖胺与人体细胞的固有成分——透明质酸极相似,因而具有良好的亲和性,对人体不产生排斥反应。
同时,壳聚糖还具有很强的吸附性和螯合作用。遇酸溶解的壳聚糖呈凝胶状态具有很强的吸附能力。同时寡聚葡萄糖胺和葡萄糖胺的羟基受邻位氨基的影响与重金属离子产生螯合作用,螯合系数随金属原子量加大而增强。
脱乙酰度达到95%的壳聚糖,护肤品中应用并不是很多。只有一些专业进口的医学品牌,如法国美帕的壳聚糖系列产品才有添加使用。
4.4 在食品中的应用
4.4.1 絮凝剂和增稠剂
由于带氨基的壳聚糖是阳离子电解质,在溶液中对有机物悬浮颗粒有明显的絮凝效果且无毒、无味,可用于饮料及酒类的除浊澄清,防止醋、酱油沉淀。作为絮凝剂和增稠剂添加到蛋黄酱、花生酱、芝麻酱、玉米糊罐头、含有沙司的罐装食品、奶油代用品、酸性奶油、酸性奶油代用品中,增稠效果明显并可使产品长期贮存不变质,延长货架期。
4.4.2 防腐保鲜
壳聚糖衍生物如N-羧丁基壳聚糖对细菌、霉菌、酵母菌均具有较强的抑制作用,其中对大肠杆菌、枯草杆菌、毛霉、根霉具有更强烈的抑制作用。壳聚糖衍生物具有良好的水溶性和广谱抗菌性,无毒无害。在食品、果蔬、农产品的防腐保鲜上有广泛的应用。将壳聚糖与乳酸钙或醋酸钙制成一种水溶性保鲜剂具有高杀菌活性、安全无毒。
壳聚糖还应用在草莓、苹果、猕猴桃、鸡蛋、柚桔、苹果汁、肉类、水产品的防腐保鲜中效果很好。
4.4.3 食品包装膜
将壳聚糖与淀粉、水混合均匀制成薄膜、干燥,经碱溶液处理,可制成壳聚糖-淀粉合成食品包装膜,此膜可食,无毒,耐油,抗张强度高,不溶于冷、热水,可用于包装固体、半固体和液体食品。该膜能自动生物降解,无白色环境污染。
4.4.4 固定化酶载体
将壳聚糖醋酸溶液喷入到碱性溶液中进行凝固,经分离再生得到壳聚糖微细颗粒,此颗粒可作为固定化酶载体。被壳聚糖固定的酶可广泛应用于制糖、酿酒、造醋等食品工业。
4.4.5 保健食品
甲壳质、壳聚糖作为功能性保健食品对人类有5大功能:免疫强化功能、抑制老化、预防疾病、促进疾病痊愈和调节人体生理机能。将壳聚糖与其他成分配合使用,可研制出人类所需的新产品。如将2份壳聚糖与10份不同比例的甲酸、硫酸铁溶液反应,可制成可溶性铁-壳聚糖络合物,其补血效果优于其他补血食品。壳聚糖与油酸、亚油酸等脂肪酸按比例混合研制成壳聚糖-脂肪酸络合物,可添加到各种保健食品中。壳聚糖与果胶、卡拉胶等酸性多糖可加工成壳聚糖-酸性多糖络合盐,这种络合盐可与肉类中脂肪酸结合,不被人体吸收而制成高质量低热能减肥保健品。日本还将壳聚糖与传统的中药保健品混合作保健品出售,在市场上很受欢迎。
4.5 壳聚糖在农业中应用
4.5.1 壳聚糖种衣剂
种子包衣是近年来研制出的一项加工处理种子的新技术。种衣剂在种子周围形成防治病虫的保护屏障,保证种子正常吸水发芽生长和药肥缓慢释放,延长药效期。壳聚糖处理后的种子,其中的Chitinase 的活性可提高1.5倍。具有良好的防病、防虫和促进作物生长作用,即简便易行,又使杀虫剂对使用者和环境污染减小,是理想的环保型杀虫剂,在生产上得到广泛应用。
4.5.2 可降解壳聚糖地膜
利用甲壳质的成膜性及生物降解性,可制成具有良好粘附性、通透性和一定抗拉强度的农用地膜,代替现在广泛使用的聚乙烯地膜,克服了聚乙烯地膜板结土壤,不利作物生长的缺点,并且避免了白色污染。
4.5.3 饲料添加剂
利用甲壳质和壳聚糖作鸡饲料添加剂,能使小鸡明显增重;做鱼饵料添加剂对鱼有显著的增重作用;在猪饲料中添加壳聚糖,可以提高育肥猪的瘦肉率。
参考文献:
[1]杨冬梅,缪进康,黄明智. 天然生物材料-甲壳素和壳聚糖的开发及应用[J].化学工业与工程,1999,16(6):335-340.
[2]胡继飞. 甲壳质及其衍生物的开发利用[J].生物技术,1994(4):45-47.
[3]赵国俊,姜涌明,孙龙生.不同来源壳聚糖的基本特性及红外光谱研究[J].功能高分子学报,1998,11(3):403-407.
[4]郭开宇,赵谋明.甲壳素/壳聚糖的研究进展及其在食品工业中的应用[J].食品与发酵工业,vol.26 No.1
[5]张 虎,杜昱光.壳聚糖酶的研究进展[J].化学通报,1999(5):32-35.
[6]梁 亮,崔英德,罗宗明. 微波新技术制备壳聚糖的研究[J].广东工业大学学报,1999,16(1):63-65,81
[7]陈海燕.微波法制取壳聚糖[J].中国水产,1999(2):45-46.
[8]陈 晰.微生物培养法生产壳聚糖的初步研究[J].食品科学,1999(7):22-24.
[9]WHITE S A,FARINA P R,FULTION I. Production and isolation of chitosan from Mucor rouxii[J]. Appl Environ Microbiol, 1979,38:323-328.
[10]MCGAHREN W J, PERKINSON G A, GROWICH J A, et al. Chitosan by fermentation[J]. Proc Biochem, 1984,19:88-90.
[11]魏 光,李兆兰. 从蓝色犁头霉中提取壳聚糖的初步研究[J].安徽师范大学学报:自然科学版,1998, 21(3):227-231,234.
[15]赵继伦,王红林. 利用柠檬酸废菌体制备壳聚糖的工艺研究[J]. 工业微生物,1999,29(2):33-37.
[12]Majeti NV,Kumar R.A州w of clfitin and chitosan applications[J].Reac Func Polym,2000,46:1.
[13] Sinlm VR,Singla’AK,Wadhawan S,et al.Chitesan mierespheres as a potential carrier for drugs [J].Int J Pharm,2004,274:1.
[14]Hirofuml T,HinⅫitan Y,Yod[Iiaki K.Mucoadhesive nanoparticulate systems for pepfide drug delivery[J].Adv Drug Ddliv Rev,2001,47:39.
[15] van der Lubben IM,Verhoef JC,Borchard G,d 02.Chitesan forⅫ一cesal vaccination[J].Adv Drug Ddliv Rev,2001,52:139.
[16] Krishnendu R.Chitosan—DNA mmoparfieles:synthesis,eharacterizafian,
subcellular transport and oral delivery 0f genetic vaccines[D].
Baltimore the Johns aopkius University,1999.
[21]王中和,陆顺娟,胡海生. 低分子壳聚糖对癌症放疗患者免疫功能的影响[J].首都医科大学学报,
1997,18:79-81
[22]MINAMI S. Mechanism of wound healing acceleration by chitin and chitosan[J]. Jap J Vet Res,1997,44(4):218-219.
[17]Kotze A F,Thanon M M, Luebetaen H H, et al. Enhancement of paracellular drug transport with highly quaternized N-trimethyl chitosan chloride in neutral environments: in vivo evaluation in intestinal cells (caro-2)[J].J Pharm Sci, 1999,88(2):253-257.
[18]Tozaki H ,Fujita T, Odorida T, et al. Colon-specific dwelivery of R68070, a new thromboxanesynthase inhibitor, using chitosan capsules; therapeutic effects against 2,4,6-trinitrobenzene sulfonic acid-induced ulcerative colitis in rats[J]. Life Sci,1999,64(13):1155-1162.
[19]Khairoun I,Deriessens F C M, Boltong M G, et al. Addition of cohesion promoters to calcium phosphate cements[J]. Biomaterials, 1999,20(4):393-398.
[20]方波,宋道云,陈鸿雁等.微球型壳聚糖胺基吸附剂的制备及性能[J].化工科技,2000,8(3):20-23.
[21] 徐鑫,王静.甲壳质和壳聚糖的开发及应用[J].哈尔滨工业大学学报,Feb.2002vol,34 No,1
[22] 张良,张岫竹 ,张连阳,王正国. 美军战术区战伤救治的变革[J].中华灾害救援医学.2017年8月第5卷第8期.

