微量元素的概念(微量元素概念是什么意思)
本篇内容在知识地图中的位置
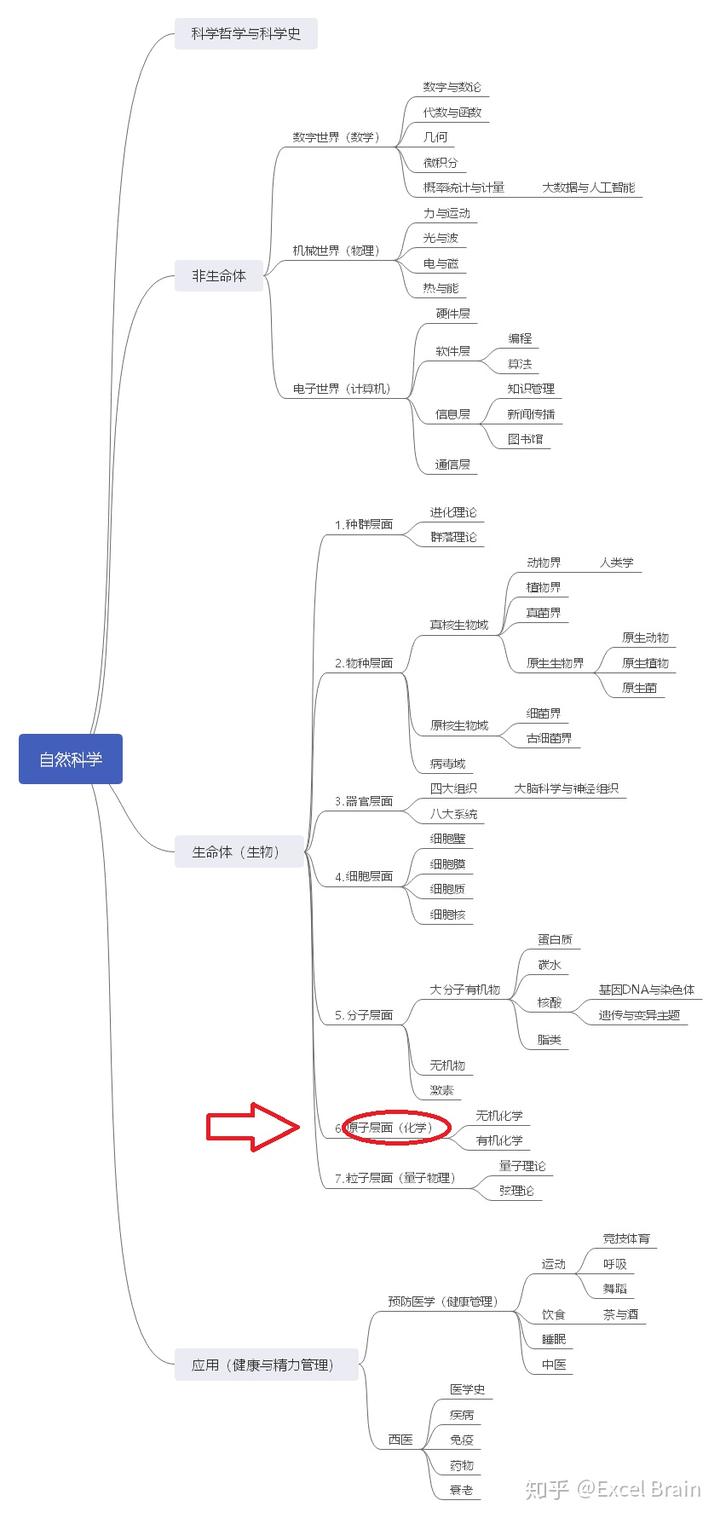

参考文本:
元素 定义:具有相同核电荷数(质子数)的一类原子的总称 #同种元素。 质子数相同中子数不一定相同。
核素 具有一定质子数和中子数的原子
同位素 质子数相同 但是中子数不同的同一类原子 1.同位指的是质子数相同#在元素周期表中的位置相同
2.许多元素都有同位素
3同位素质量数不同 ,但是核电荷数相同,所以核外电子结构相同 同位素物理性质不同,化学性质完全相同
4.用途 “14 2 3
6C 考古 1H 1H 做氢弹等 #日常生活考古治疗恶性肿瘤等”
氕氘氚 中子数分别是0 1 2分别是氢 重氢 超重氢
元素性质的周期性(统论) 元素周期表 发现 门捷列夫
关系 核外电子数=质子数=核电荷数=原子序数
排列方式: 按原子序数的大小从左到右排成横行(周期),同一横行最外层电子数相同的原子拍一竖行(族)
周期 (7) 3个短周期 4个长周期
族 18个纵列 16个族 7个主族A7个副族B1个0族1个第八族(8910)
书写方式,举例 K 第四周期第ⅠA 族
电子层数决定周期序数, 最外层电子数决定族序数 在元素周期中,随着原子序数的增加,原子半径逐渐增大。原子核对最外层电子引力越来越弱,元素失电子能力越来越强,得电子能力越来越弱。单质还原性越来越强,氧化性越来越弱。金属性越来越强。非金属性越来越弱。
碱金属元素 包括 :锂钠钾铷铯钫 Li Na K Rb Cs Fr 第ⅠA族
性质 物理性质 从Li 到Fr 硬度小且越来越小, 密度较小呈增大趋势,熔沸点降低
注意:Li保存在液态石蜡中;Na保存在煤油中
化学性质 碱金属元素最外层电子数都是1 (化学性质相似) 与氧气反映 4Li+O2加热2LI2O
2Na+O2加热Na2O2
K +O2 加热KO2(超氧化钾)
与水反映(非金属单质) 2Li +2H2O =2LiOH +H2↑#浮 不熔 游 响 红
2Na +2H2O =2NaOH +H2↑#浮 熔 游 响 红
2K+2H2O =2KOH +H 2↑#浮 熔 游 响 燃 爆 红
2M+2H2O =2MOH +H2↑(M 为碱金属元素)
易失去最外层电子 ,单质的还原性强
1.相似性 #最外层电子都是1
2.递变性 – 随着原子序数的增加 原子半径逐渐增大 原子核对最外层电子的引力逐渐减弱 容易失去最外层电子 失电子能力增强 单质还原性增强
检验元素金属性强弱的方法 1.置换反应
2.最最高价氧化物的水化物(氢氧化物)的碱性强弱
3单质与水(酸)置换出氢气的难易程度
卤族元素 包括:氟氯溴碘砹 F Cl Br I At 第ⅦA族
性质 物理性质 从F到At 密度越来越大 氧化性越来越弱 熔沸点越来越高颜色越来越深
注意:F Cl 是气体Br 是液体I At 是固体
化学性质 与H2反映 H2+F2=2HF (稳得一批)
H2+Cl2光照或点燃 2HCl (不大稳定 光照容易分解)
Br2+H2加热2HBr (没HCl稳定)
I2 +H2可逆2H I (是可逆反应)
X 2+H2=2H X (X 是卤族元素)
与水反应 2F2+2H20=4HF +O2 2X2+2H2O=4HX+O2
Cl2+H2O 可逆符号HCl +HClO (Cl Br I )
和碱反映 X2+NaOH =NaX+NaXO+H2O # X Cl Br I
1.相似性#最外层电子数都是7
2.递变性 F →I 氧化性越来越弱 ,还原性越来越强,越来越稳 随着原子序数的增加 原子半径逐渐增大 原子核的引力越来越弱 得电子能力越来越弱 单质的还原性越来越强 氧化性越来越弱 越来越稳定
检验元素非金属性强弱的方法 1.单质间的置换反应
2.生成气态氢化物的难易程度,(稳定性)
3.最高价氧化物及其水化物的酸性强弱来判断
主族元素 主族元素性质的规律
主族的金属元素与非金属元素
过渡元素 过渡元素的性质
其他重要的过渡元素
内过渡元素:镧系和锕系
元素同期表的发展史 对元素周期表的探索
现代元素周期表
元素周期表的使用 元素周期表和原子结构的关系
元素的物理状态和分类
半导体及其应用
元素周期表 原子序数 符号 中文 读音 相对原子质量 价电子 “常见化合价:一价氢氟钾钠银 二价氧钡钙镁锌
三铝四硅五价磷 二四六硫二四碳
一二铜汞二三铁一五七氯要记清” 分类 英文名 简介
1 H 氢 qīng 1.008 1s1 +1、-1 主族、非金属 Hydrogen 密度最小,同位素为氕、氘和氚
2 He 氦 hài 4.003 1s2 0 主族、非金属、稀有气体 Helium 最难液化,稀有气体,由中国学者成功制得氦化合物Na2He
3 Li 锂 lǐ 6.941 2s1 1 主族、金属、碱金属 Lithium 性质活泼
4 Be 铍 pí 9.012 2s2 2 主族、金属、碱土金属 Beryllium 最轻碱土金属元素
5 B 硼 péng 10.81 2s2、2p1 3 主族、非金属 Boron 单质硬度仅次于金刚石的非金属元素
6 C 碳 tàn 12.01 2s2、2p2 无机+2、+4、-4,有机不规则 主族、非金属 Carbon 硬度最高(金刚石),细胞干重中含量最高
7 N 氮 dàn 14.01 2s2、2p3 -3、 +1 、+2、 +3、 +4、+5 主族、非金属 Nitrogen 空气中含量最多的元素
8 O 氧 yǎng 16 2s2、2p4 -2、-1 主族、非金属 Oxygen 地壳中最多,生物体内最多
9 F 氟 fú 19 2s2、2p5 -1 主族、非金属、卤素 Fluorine 最活泼的非金属,单质不能被氧化
10 Ne 氖 nǎi 20.18 2s2、2p6 0 主族、非金属、稀有气体 Neon 稀有气体
11 Na 钠 nà 22.99 3s1 1 主族、金属、碱金属 Sodium 活泼,与空气或水接触发生反应,只能储存在煤油或稀有气体中
12 Mg 镁 měi 24.31 3s2 2 主族、金属、碱土金属 Magnesium 轻金属之一
13 Al 铝 lǚ 26.98 3s2、3p1 3 主族、金属 Aluminium 地壳里含量最多的金属
14 Si 硅 guī 28.09 3s2、3p2 +4、-4 主族、非金属 Silicon 地壳中含量仅次于氧
15 P 磷 lín 30.97 3s2、3p3 -3、+3、+5 主族、非金属 Phosphorus 白磷有剧毒且在常温下可以自燃
16 S 硫 liú 32.06 3s2、3p4 -2、+4、+6 主族、非金属 Sulphur 质地较软且轻。与氧气燃烧反应形成有毒的二氧化硫
17 Cl 氯 lǜ 35.45 3s2、3p5 -1、+1、+3、+4、+5、+7 主族、非金属、卤素 Chlorine 有毒、活泼
18 Ar 氩 yà 39.95 3s2、3p6 0 主族、非金属、稀有气体 Argon 稀有气体,在空气中含量最多的稀有气体
19 K 钾 jiǎ 39.1 4s1 1 主族、金属、碱金属 Potassium 比钠活泼
20 Ca 钙 gài 40.08 4s2 2 主族、金属、碱土金属 Calcium 骨骼主要组成成分
21 Sc 钪 kàng 44.96 3d1、4s2 3 副族、金属 Scandium 一种柔软过渡金属,常与钆、铒混合存在
22 Ti 钛 tài 47.87 3d2、4s2 +3、+4 副族、金属 Titanium 能在氮气中燃烧,熔点高
23 V 钒 fán 50.94 3d3、4s2 +3、+5 副族、金属 Vanadium 高熔点稀有金属
24 Cr 铬 gè 52 3d5、4s1 +3、+4、+6 副族、金属 Chromium 硬度最高的金属
25 Mn 锰 měng 54.94 3d5、4s2 区间[-3,+7]的整数 副族、金属 Manganese 在地壳中分布广泛
26 Fe 铁 tiě 55.85 3d6、4s2 +2、+3、+6 Ⅷ族、金属 Iron 地壳含量第二高的金属,单质产量最高,有磁性
27 Co 钴 gǔ 58.93 3d7、4s2 +2、+3 Ⅷ族、金属 Cobalt 同位素60Co被应用于X光发生器中,有磁性
28 Ni 镍 niè 58.69 3d8、4s2 +2、+3 Ⅷ族、金属 Nickel 有磁性和良好可塑性
29 Cu 铜 tóng 63.55 3d104s1 +1、+2 副族、金属 Copper 人类发现较早的金属之一,可塑性很好
30 Zn 锌 xīn 65.39 3d10、4s2 2 副族、金属 Zinc 人体需要的微量元素
31 Ga 镓 jiā 69.72 3d10、4s2、4p1 3 主族、金属 Gallium 熔点低沸点高
32 Ge 锗 zhě 72.64 3d10、4s2、4p2 4 主族、金属 Germanium 是一种重要的半导体材料
33 As 砷 shēn 74.92 4s2、4p3 -3、+3、+5 主族、非金属 Arsenic As2O3(即砒霜)剧毒
34 Se 硒 xī 78.96 4s2、4p4 -2、+4、+6 主族、非金属 Selenium 可使玻璃致色为鲜红色
35 Br 溴 xiù 79.9 4s2、4p5 -1、+5、+7 主族、非金属、卤素 Bromine 活泼,单质为红棕色液体
36 Kr 氪 kè 83.8 4s24p6 2 主族、非金属、稀有气体 Krypton 稀有气体
37 Rb 铷 rú 85.47 5s1 1 主族、金属、碱金属 Rubidium 比钾活泼
38 Sr 锶 sī 87.62 5s2 2 主族、金属、碱土金属 Strontium 是碱土元素中丰度最小的元素
39 Y 钇 yǐ 88.91 4d1、5s2 3 副族、金属 Yttrium 人工合成的钇铝榴石曾被当做钻石的替代品
40 Zr 锆 gào 91.22 4d2、5s2 4 副族、金属 Zirconium 氧化物立方氧化锆为钻石的人工替代品
41 Nb 铌 ní 92.91 4d4、5s1 5 副族、金属 Niobium 铌钢被用于制作汽车外壳
42 Mo 钼 mù 95.96 4d5、5s1 +4、+6 副族、金属 Molybdenum 植物生长所需的微量元素
43 Tc 锝 dé 98 4d5、5s2 +4、+7 副族、金属 Technetium 原子序数最小的放射性元素
44 Ru 钌 liǎo 101.1 4d7、5s1 +1、+4、+8 Ⅷ族、金属 Ruthenium 硬而脆呈浅灰色的多价稀有金属元素
45 Rh 铑 lǎo 102.9 4d8、5s1 +3,+4 Ⅷ族、金属 Rhodium 现代珠宝制作过程进行表面处理的必须元素
46 Pd 钯 bǎ 106.4 4d10 +2、+4 Ⅷ族、金属 Palladium 被应用于酒精检测中
47 Ag 银 yín 107.9 4d10、5s1 1 副族、金属 Silver 贵金属,曾经是全球范围内的硬通货,导电性最好
48 Cd 镉 gé 112.4 4d10、5s2 2 副族、金属 Cadmium 重金属,过量摄入会导致痛痛病
49 In 铟 yīn 114.8 5s2、5p1 3 主族、金属 Indium 可塑性强,有延展性,115In是主要核素,有放射性
50 Sn 锡 xī 118.7 5s2、5p2 +2、+4 主族、金属 Tin 人类最早发现应用的元素之一,被用于制造容器
51 Sb 锑 tī 121.8 5s2、5p3 -3、+3、+5 主族、金属 Antimony 熔点低,被用于制作保险丝
52 Te 碲 dì 127.6 5s2、5p4 -2、+4、+6 主族、非金属 Tellurium 密度最大的非金属
53 I 碘 diǎn 126.9 5s2、5p5 -1、+5、+7 主族、非金属、卤素 Iodine 活泼,甲状腺所需的微量元素
54 Xe 氙 xiān 131.3 5s2、5p6 +4、+6、+8 主族、非金属、稀有气体 Xenon 稀有气体
55 Cs 铯 sè 133 6s1 1 主族、金属、碱金属 Cesium 活泼
56 Ba 钡 bèi 137.3 6s2 2 主族、金属、碱土金属 Barium 硫酸钡被应用于钡餐透视(检查是否胃穿孔)
57 La 镧 lán 139 5d1 6s2 3 副族、金属、镧系 Lanthanum 第一个镧系元素
58 Ce 铈 shì 140 4f1 5d1 6s2 +3、+4 副族、金属、镧系 Cerium 用来制造打火石
59 Pr 镨 pǔ 141 4f3 6s2 3 副族、金属、镧系 Praseodymium 英文名称最长
60 Nd 钕 nǚ 144 4f4 6s2 3 副族、金属、镧系 Neodymium 磁性强
61 Pm 钷 pǒ 145 4f5 6s2 3 副族、金属、镧系 Promethium 有放射性
62 Sm 钐 shān 150.5 4f6 6s2 3 副族、金属、镧系 Samarium 磁性强
63 Eu 铕 yǒu 152 4f7 6s2 3 副/金/镧 Europium 活泼,能放出红光
64 Gd 钆 gá 157 4f7 5d1 6s2 3 副/金/镧 Gadolinium 未配对电子达到上限
65 Tb 铽 tè 159 4f9 6s2 3 副/金/镧 Terbium 通电时改变形状
66 Dy 镝 dī 162.5 4f10 6s2 3 副/金/镧 Dysprosium 英文名称源自“很难得到”
67 Ho 钬 huǒ 165 4f11 6s2 3 副/金/镧 Holmium 银白色,质软,可用来制磁性材料
68 Er 铒 ěr 167 4f12 6s2 3 副/金/镧 Erbium 银灰色,质软,可用来制特种合金,激光器等
69 Tm 铥 diū 169 4f13 6s2 3 副/金/镧 Thulium 银白色,质软,可用来制X射线源等
70 Yb 镱 yì 173 4f14 6s2 +2、+3 副/金/镧 Ytterbium 银白色,质软,可用来制特种合金,也用作激光材料等
71 Lu 镥 lǔ 175 4f14 5d1 6s2 3 副/金/镧 Lutetium 银白色,质软,可用于核工业
72 Hf 铪 hā 178.5 5d2 6s2 4 副/金 Hafnium 银白色,熔点高。可用来制耐高温合金,也用于核工业等
73 Ta 钽 tǎn 181 5d3 6s2 5 副/金 Tantalum 钢灰色,耐腐蚀质硬,熔点高。可用于航天工业及核工业
74 W 钨 wū 184 5d4 6s2 +4、+6 副/金 Tungsten 稳定元素中熔点最高
75 Re 铼 lái 186 5d5 6s2 7 副/金 Rhenium 最晚被发现的稳定元素
76 Os 锇 é 190 5d6 6s2 +4,+6,+8 副/金 Osmium 密度最大的金属
77 Ir 铱 yī 192 5d7 6s2 +3,+4、+6、+9 副/金 Iridium 熔点高,质硬而脆。可用来制科学仪器等
78 Pt 铂 bó 195 5d9 6s1 +2,+4 副/金 Platinum 被应用于珠宝首饰中的贵金属,俗称铂金
79 Au 金 jīn 197 5d10 6s1 +1、+3 副/金 Gold 化学性质极稳定,人类最早发现及应用的贵金属,全球硬通货
80 Hg 汞 gǒng 200.6 5d10 6s2 +1、+2 副/金 Mercury 唯一一种在常温(25°C)下为液态的金属
81 Tl 铊 tā 204.5 6s2 6p1 3 主/金 Thallium 银白色,质软。可用来制合金等。铊的化合物有毒
82 Pb 铅 qiān 207 6s2 6p2 +2、+4 主/金 Lead 密度大,熔点低,对人体有毒性。许多化妆品中必须含有的元素
83 Bi 铋 bì 209 6s2 6p3 +3、+5 主/金 Bismuth 合金熔点很低,可用来做保险丝和汽锅上的安全塞等
84 Po 钋 pō 209 6s2 6p4 -2、+6 主/金 Polonium 放射
85 At 砹 ài 210 6s2 6p5 5 主/非/卤 Astatine 放射、活泼
86 Rn 氡 dōng 222 6s2 6p6 2 主/非/稀 Radon 放射
87 Fr 钫 fāng 223 7s1 1 主/金/碱 Francium 放射(注:放射性虽短但仍然存在)
88 Ra 镭 léi 226 7s2 2 主/金/碱土 Radium 放射
89 Ac 锕 ā 227 6d1 7s2 3 副/金/锕 Actinium 放射
90 Th 钍 tǔ 232 6d2 7s2 4 副/金/锕 Thorium 放射
91 Pa 镤 pú 231 5f2 6d1 7s2 5 副/金/锕 Protactinium 放射
92 U 铀 yóu 238 5f3 6d1 7s2 +3、+4,+6 副/金/锕 Uranium 放射,同位素铀235被用于制作原子弹
93 Np 镎 ná 237 5f4 6d1 7s2 +5、+7 副/金/锕 Neptunium 放射
94 Pu 钚 bù 244 5f6 7s2 +4、+6、+8 副/金/锕 Plutonium 放射,用于制作原子弹
95 Am 镅 méi 243 5f7 7s2 +3、+5、+7、+8 副/金/锕 Americium 人造 放射
96 Cm 锔 jú 247 5f7 6d1 7s2 +3、+6、+7 副/金/锕 Curium 人造 放射
97 Bk 锫 péi 247 5f9 7s2 +3、+5 副/金/锕 Berkelium 人造 放射
98 Cf 锎 kāi 251 5f10 7s2 +3、+5 副/金/锕 Californium 人造 放射,最贵金属
99 Es 锿 āi 252 5f11 7s2 3 副/金/锕 Einsteinium 人造 放射
100 Fm 镄 fèi 257 5s12 7s2 3 副/金/锕 Fermium 人造 放射
101 Md 钔 mén 258 5f13 7s2 3 副/金/锕 Mendelevium 人造 放射
102 No 锘 nuò 259 5f14 7s2 +2、+3 副/金/锕 Nobelium 人造 放射
103 Lr 铹 láo 260 5f14 7s27p1 3 副/金/锕 Lawrencium 人造 放射
104 Rf lú 261 6d2 7s2 4 副/金 Rutherfordium 人造 放射
105 Db dù 262 6d3 7s2 5 副/金 Dubnium 人造 放射
106 Sg xǐ 263 6d4 7s2 6 副/金 Seaborgium 人造 放射
107 Bh bō 264 6d5 7s2 7 副/金 Bohrium 人造 放射
108 Hs hēi 265 6d6 7s2 8 副/金 Hassium 人造 放射
109 Mt 鿏 mài 266 6d7 7s2 0 副/金 Meitnerium 人造 放射
110 Ds dá 269 6d8 7s2 0 副/金 Darmstadtium 人造 放射
111 Rg lún 272 6d9 7s2 0 副/金 Roentgenium 超重元素
112 Cn 鿔 gē 277 6d10 7s2 0 副/金 Copernicium 超重元素
113 Nh 鉨 nǐ 286 5f146d107s27p1 +3,+1 主/金 Nihonium 不稳定的超重元素,人造 放射
114 Fl fū 289 5f146d107s27p2 ,0,+3 主/金 Flerovium 第一种表现出惰性气体特征的超重元素,人造 放射
115 Mc 镆 mò 289 5f146d107s27p3 +1,+3 主/金 Moscovium 人工合成的放射性金属元素,人造 放射
116 Lv lì [18] 293 5f146d107s27p4 4 主/金 Livermorium 人工合成的放射性化学元素,人造 放射
117 Ts 石田 tián 294 5f146d107s27p5 -1 主/非/卤 Tennessine 卤族元素,人造 放射
118 Og 气奥 ào 294 5f146d107s27p6 主/非/稀 Oganesson 人工合成的稀有气体元素,人造 放射
参考书 决战元素周期表
走进奇妙的元素周期表
第一章元素周期表上究竟写了什么?
第二章通过元素周期表解读宇宙
第三章不断进行化学反应的人体
第四章为什么我们能“动”?
第五章稀土元素并非局外人
第六章美妙的稀有气体与气体的世界
第七章通过周期表判断元素是否有益健康
诗意的原子
致命元素:毒药的历史
汞、砷、铅
元素的盛宴
第一部分定位:行行又列列 1.位置决定命运/3
2.亲密双胞胎与黑羊:元素家谱/18
3.元素周期表上的科隆群岛/29
第二部分制造原子,破坏原子 4.原子从哪里来:“我们是群星之子”/43
5.战争年代的元素/54
6.完善周期表⋯⋯砰的一声/66
7.在冷战中扩展周期表/78
第三部分周期之惑:疑难初现 8.从物理学到生物学/93
9.毒药协会:“哎哟喂”/105
10.带两个元素,早上打电话叫醒我/115
11.元素也会骗人/128
第四部分元素与人性 12.元素与政治/141
13.元素与货币/156
14.元素与艺术/169
15.元素与疯癫/183
第五部分元素科学的今天与明天 16.零度以下的化学/199
17.光辉的球体:泡泡与科学/213
18.精确到荒唐的工具/227
19.超越元素周期表/240

